随着制药产业的快速发展,生产工艺的多元化,其排放的废水水质也日趋复杂。制药废水具有成分复杂、高盐、可生化性差且有机物含量高等特点,这种废水中所含的大部分污染物属于难降解有机物,对水体中的微生物具有一定的危害与毒性,并且在环境中残留时间较长。
我国排放标准日趋严格,企业在处理过程中遇到很大挑战,高盐制药废水是我国最难处理废水之一,传统的二级生化处理技术很难达到国家排放标准,废水排入收纳水体,不仅严重危害了自然环境,危害人体健康,也制约了企业的经济发展。生物法是处理该类废水最常用且经济的方法,但高盐和复杂有机物会对微生物造成毒害作用,难以达到处理目标,而采用预处理可以有效降低其危害作用,提高可生化性。
在Fenton高级氧化反应中,通过其・OH的强氧化性可以将水体中的部分有机物氧化分解,最后生成H2O和CO2,这种方法适用于大部分水样,且反应迅速,氧化能力高。杜小龙等采用Fenton技术对抗生素废水进行处理,处理后的水质强化了生化处理能力,达到了排放标准。
单宁等对印染废水进行Fenton预处理,经处理后的水质可满足印染废水排放标准。本文采取Fenton氧化法对高盐制药废水进行预处理,通过单因素实验和正交试验确定最佳反应条件以及对废水的预处理效果,为制药废水处理的达标排放提供一定的技术参考。
1、实验材料与方法
1.1 水源
实验所选用的水源来自于某工业园区污水处理厂进水,该厂主要承接某制药企业二级处理后的出水。
实际废水特点:颜色微黄,无刺激性气味,COD含量为1130.60mg/L,废水中的盐度主要来自以NaCl为主的无机盐,CI含量为10.53mg/L。
1.2 实验材料
本研究所用主要药品及试剂见表1。

本研究所需主要仪器及设备见表2。

1.3 实验方法
取某工业园区污水处理厂进水,分别进行单因素(列出来)和正交试验,本研究主要以COD的处理效果为目标进行分析。主要分析项目及测定方法见表3。

正交试验设计见表4。
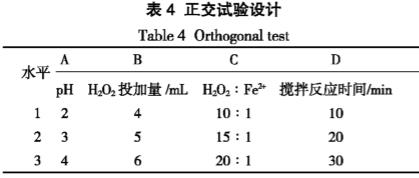
在500mL的烧杯中加入一定量的实际废水,通过浓硫酸和氢氧化钠调节水体的pH,控制反应时间、硫酸亚铁和过氧化氢的投加量,反应结束后取上清液测定COD。
对Fenton处理前后的水质分别进行GC-MS分析。上样前,分别用3mL甲醇、3mL去离子水活化watersC18固相萃取小柱。上样后,分别用3mL去离子水清洗杂质,3mL甲醇洗脱,收集洗脱液经氮气吹干后用100μL甲醇复溶进样。
GC-MS实验条件:进样口250℃,不分流,进样体积为1μL,柱流量为1mL/min,以氦气为载气,起始50℃保持3min,10℃/min升温到210℃后保留3min,10℃/min升温到300℃后保留5min,离子源温度为230℃,接口温度为250℃,溶剂延迟时间3min,电子轰击能量70eV,采集M/Z范围25-900。
2、结果与讨论
2.1 单因素实验
2.1.1 初始pH值对COD去除率的影响
控制H2O2投加量为5mL,H2O2:Fe2+为5:1,搅拌反应时间10min,以初始pH为不同变量进行单因素实验,用1.0mol/L硫酸对初始pH值进行调节,改变pH值分别为2、3、4、5和6,分析初始pH对COD去除率的影响,并确定最佳初始pH值。初始pH对COD去除效果影响如图1所示。

由图1可知,当初始pH为3时对COD的去除效果最好,达到54.75%。在酸性条件下,pH值<3时,Fenton氧化对有机物的去除效果随着pH的上升而提高;当pH值>3时,COD的去除率大幅度下降。
在pH较低时,水体中过多的氢离子会抑制反应Fe3+H2O2→Fe2++HO2・+H+的进行,对Fe2+的催化再生产生一定影响,对水体中的有机物去除不利。但过高的pH会使H2O2不稳定,.OH降低,同样造成有机物去除效果的降低。
2.1.2 H2O2投加量对COD去除率的影响
控制初始H2O2:Fe2+为5:1,pH值为3,搅拌反应时间10min,改变H2O2投加量(3、4、5、6和7mL),考察H2O2投加量对高盐废水中有机物的降解效果影响,确定最佳的H2O2投加量,H2O2对COD去除效果影响如图2所示。
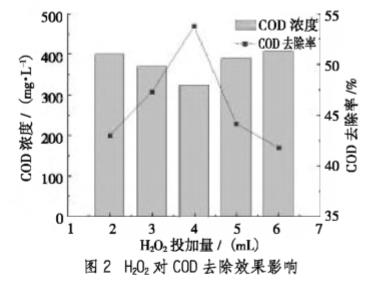
由图2可知,当初始H2O2投加量在不超过5mL时,Fenton氧化反应对有机物的降解随着投加量的增加而提高,当投加量高于5mL时,COD的去除率明显降低。在H2O2投加量为5mL时,COD去除效果最好,为53.75%。
H2O2投加量在不超过5mL时,水体中的・OH增多,可以加速水体中有机物的降解,但随着投加量过多,当H2O2投加量高于5mL时,过量的H2O2与・OH反应生成H2O和HO2,影响Fenton氧化反应过程,使COD去除率降低。
2.1.3 H2O2/Fe2+对COD去除率的影响
控制反应的初始pH值为3,H2O2投加量5mL,搅拌反应时间为10min,以H2O2/Fe2+为不同变量进行单因素实验,改变硫酸亚铁投加量(H2O2:Fe分别为1:1、5:1、10:1、15:1和20:1),根据COD去除率确定单因素实验条件下对COD去除效率最高的H2O2:Fe2+,并分析H2O2/Fe2+对COD去除率的影响,H2O2:Fe2+对COD去除效果影响如图3所示。

由图3可知,随着H2O2:Fe2+值增加,水体中的有机物去除效果大幅度提高,其中H2O2:Fe2从1:1到5:1,COD的去除率明显上升,从31.15%上升到53.75%,HO2:Fe2+从5:1到20:1,
COD的去除率上升较为缓慢,当H2O2:Fe2+为20:1时,COD去除效果最佳,这时COD去除率为69.88%。当H2O2:Fe2t在比值很小时,即Fe2+含量较高的时候,反应剩余的Fe2+会与・OH发生氧化还原反应,生成Fe#和OH-,抑制了有机物降解。
2.1.4 搅拌反应时间对COD去除率的影响
控制H2O2投加量为5mL,H2O2:Fe2+为5:1,pH值为3,改变搅拌反应时间(分别为15、20、25、30和35min),根据对COD的去除效果确定最佳搅拌反应时间,反应时间对COD去除效果影响如图4所示。
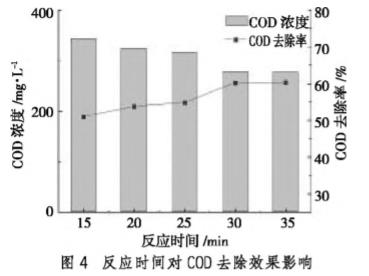
由图4知,水体中的有机物降解率随着反应时间的延长而逐渐增加,30min后去除率上升缓慢,持平缓状态。其中在反应时间为25min时,COD的去除率为54.82%,反应时间为30min时,COD的去除率为60.20%,反应时间为35min时,COD的去除率为60.34%,考虑到运行时间已经运行成本等问题,30min为最佳反应时间。
2.2 正交实验
影响Fenton实验结果的因素较多,本实验根据制药废水处理的实际工程应用,考虑初始pH值、H2O2:Fe2+、H2O2用量和反应时间4个主要因素进行研究,正交试验结果见表5。
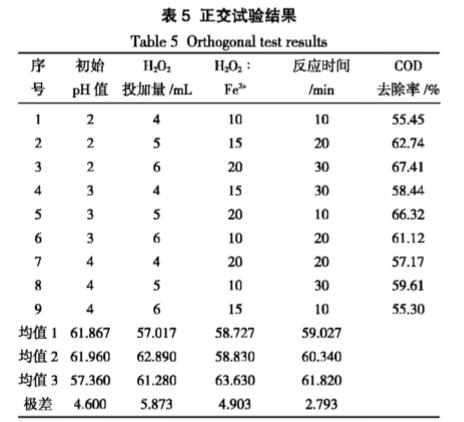
由表5可知,在Fenton氧化中各个单因素对水体中有机物的降解影响程度:H2O2投加量>H2O2:Fe2+>初始pH值>反应时间。通过正交实验确定了Fenton氧化的最佳反应条件:pH值为3、H2O2投加量为5、H2O2:Fe2+为20:1、反应时间为30min。
2.3 有机物分析
通过GC-MS联机自动检索,对色谱图中出峰物质进行定性分析,得到了经Fenton处理前后废水中有机物质的种类及含量。制药废水出水总粒子流色谱图如图5所示。

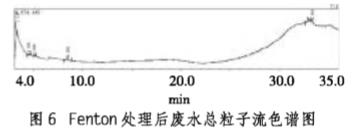
Fenton处理后废水总粒子流色谱图如图6所示。
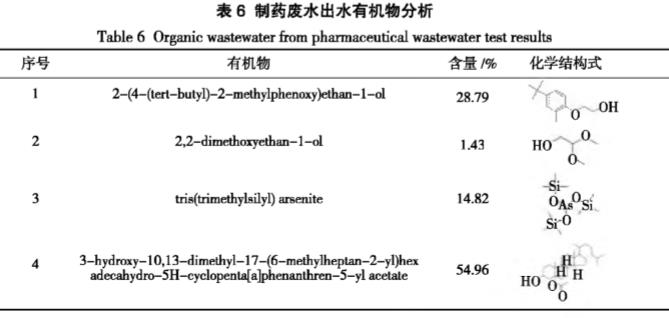
制药废水出水有机物分析见表6。
Fenton处理后废水有机物分析见表7。

由表6~7可知,制药废水出水中有机物成分复杂,种类繁多。其中园区污水处理厂进水中的有机物主要有4种,包括苯系物、脂类、醇类等,经过Fenton氧化处理后的水样中有机物种类增加,但是大部分大分子有机物转变为小分子有机物,同时部分苯系物得到了降解。由此可见,经Fenton氧化处理后的污染物有机组分产生了变化,这对后续的生化处理具有一定的积极作用。
2.4 成本分析
根据目前市场价格98%的浓硫酸300元/t,工业用30%过氧化氢2000元/t,七水硫酸亚铁200元/t,计算出采用Fenton氧化处理废水的试剂成本为8.13元/t。
3、结论
本实验采用Fenton氧化法对高盐制药废水出水进行处理并取得了良好的处理效果,其实验结果如下:
(1)单因素实验确定Fenton高级氧化法对高盐制药废水处理的最佳初始条件:pH值为3、H2O2(30%)投加量为5mL、H2O2:Fe2+为20:1、反应时间为30min。
(2)在单因素的基础上进行正交试验,表明各因素对COD去除效果的影响程度为H2O2投加量>H2O2:Fe2+>初始pH值>反应时间,在最佳条件下对有机物去除率达67.41%。
(3)经Fenton处理后的废水有机物种类与浓度均发生了变化,部分大分子有机物转化为小分子有机物。通过实验结果与成本估算,采用Fenton氧化对高盐制药废水进行预处理是可行的,可以为制药废水预处理及可生化性的提高提供技术参考。(来源:河北科技大学环境科学与工程学院,石家庄高新技术产业开发区供水排水公司)
