随着我国人口的增加以及人民生活水平的提高,对工农业的发展需求也逐渐增加,因此导致水资源量在供需方面不平衡,且由此造成的水环境污染也越来越严重,据相关学者研究,解决这种现象最根本的办法就是开源节流,就是要求我们最大限度的做好废水的回收利用,向人们灌输节约用水的观念。工业的发展必须要有充足的能源供应作为保障,据报道,矿产资源是我国能源供应的主力军,从2010-2015年我国共产煤102.3亿t,2016-2017年就产煤45.6亿t,产煤量以每年8.3%的速率快速增长,近年来我国虽在不断调整能源供应的结构,目前也是多能源供应,煤炭虽是一次性能源,但由于价格低廉且产量多,在未来很长一段时间之内其主力军地位仍无其他能源可以替代。随着煤矿的不断开采,由此造成的环境污染问题也越发严重,煤矿废水具有pH值不稳定、悬浮物浓度高、盐度高、水质复杂等特点,煤矿废水的来源主要有:矿区的生活废水、煤矿矿井废水、选煤废水以及煤制气废水等,其中矿井废水主要是采矿时会扰动地下水沉,因此必须做好矿井的排水工作;选煤废水主要是日常工艺和管理过程中对煤泥水要求循环利用外排所产生的泥水,这类废水一般悬浮物浓度较高,含有大量的溶解性固体和放射性元素等;煤制气废水主要来自工艺中煤气出口的竖管和洗涤塔冷凝后的废水,这类废水具有悬浮物浓度高,有机物和无机物含量高等特点。
煤矿废水主要有酸性废水(pH<6.5)、中性废水(pH介于6.5和8.5之间)以及碱性废水(pH>8.5),但大部分的煤矿废水还是呈中性,北方地区的煤矿主要为弱碱性或者中性废水,南方地区的煤矿主要为弱酸性和中性废水,我国煤矿的矿井废水主要包括洁净废水、高悬浮物矿井废水、高盐度废水、酸性矿井废水、甚至有些含放射性物质的废水(如镭、铀),含重金属物质的矿井废水(如铁元素)等。煤矿废水处理时应根据开采规模、排水水质要求以及废水的水质特征等方面综合考虑选用最适合和经济的工艺,目前有关这方面的研究较多,应用最多的还是混凝、沉淀、过滤、消毒、反渗透、电析等方面,因煤矿废水一般具有盐度高等特点,而混凝工艺对于处理高盐度废水具有较大的优越性,近年来在这方面的研究兴起较快,针对具体煤矿特征,混凝时要求添加适宜量的混凝剂和助凝剂,用量选取的合适与否关系到废水硬度和废水中硫酸的去除效果,本文拟选取山西朔州怀仁矿区废水作为研究对象,采用自行设计的混凝工艺,研究混凝工艺处理该矿区废水需添加的混凝剂和助凝剂量最佳用量,研究结果可为进一步了解混凝工艺的处理机理提供理论参考。
1、工艺流程以及试验方法
工艺流程如图1所示。
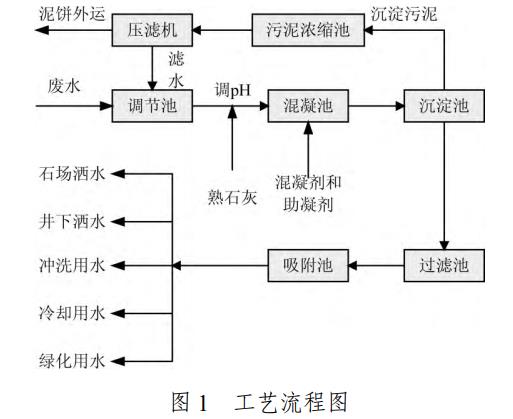
废水依次流经调节池、混凝池和沉淀池,沉淀池后对于沉淀的污泥经过污泥浓缩池浓缩后的污泥用压滤机压缩,压缩后的泥饼再外运,对于沉淀池中的水后续流经过滤池和吸附池后被循环利用,由于废水中pH为酸性,废水经调节池进入混凝池之前先加熟石灰调节pH至中性,在混凝池中添加混凝剂(PAC、PAF),本试验中所需用到的试验设备见表1。

废水水质如表2所示,其中pH采用pH试纸测,温度采用温度计测量,悬浮物(SS)采用滤膜过滤后称重,配置EDTA标准溶液,添加络黑T固体为指示剂,根据酸碱滴定原理测定水的硬度和钙元素(Ca)、镁元素(Mg)含量,添加氯化钡溶液根据沉淀滴定法测定水中硫酸根离子(SO42)含量,采用原子吸收分光光度法测定铜(Cu)元素含量,紫外分光光度法测定硝酸根(NO3-)含量,分子吸收光谱法测定铁元素(Fe)含量,采用莫尔法测定水中氯元素含量,样品检测时严格按照《水和废水监测分析方法》中相关步骤及操作规范进行。
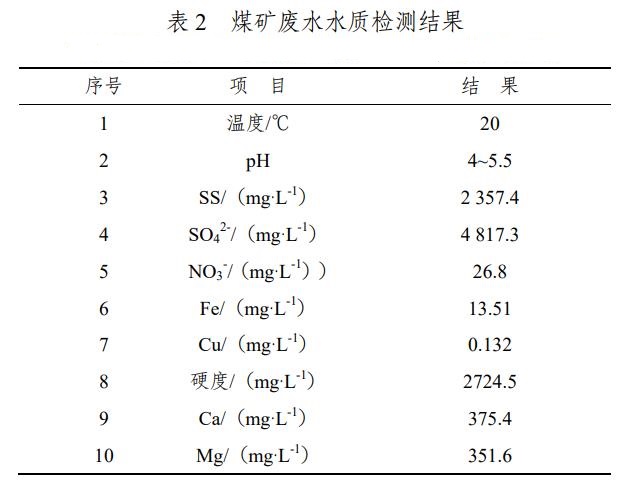
从表2可知:废水呈酸性,故应加熟石灰(Ca(OH)2)调节pH至中性,SS浓度较高、硬度、Ca、Mg和SO42-含量较高,其他检测的元素浓度值不是很高,又因Ca、Mg元素含量反映的就是硬度,故下文只对SO42-含量、SS和硬度进行分析,SS是在整个工艺过程中逐步去除,而SO42-含量和硬度主要在混凝过程中去除,故下文分析各池子内的SS浓度变化情况和混凝过程中添加的最适宜Ca(OH)2用量、混凝剂的用量。
2、结果与分析
2.1 混凝机理分析
混凝主要是在废水中添加化学物质使水中的胶体粒子或者悬浮物聚集,主要包括两个过程(凝聚和絮凝过程),其作用机理也是凝聚和絮凝机理,目前有关混凝机理方面的认识主要有:压缩双电层作用、卷扫作用和电中和作用。压缩双电层特有的结构,决定着胶体之间表面处的反离子浓度是所有位置中最大值,当颗粒之间较为分散时,颗粒之间的反离子浓度逐渐减小,直到和溶液浓度值相等,当水中添加混凝剂后,废水中的扩散层减小,反离子浓度增加,离子电位也相应的降低,因为扩散层的厚度变小了,粒子之间的排斥作用也减少了,当颗粒之间相互凝结碰撞时,因颗粒之间距离减少了,分子之间的引力也会增加,引力大于排斥力,随后颗粒之间得以聚集而沉淀;当胶体表面吸附了相关的异处离子、胶体颗粒或分子时,这些粒子可以中和自身所带的电荷,也减少了粒子之间的排斥作用,因此颗粒可以更好地聚集最终得以沉淀,同时当反离子之间相互吸附时又可以降低胶体之间表面的电荷,直至降为0,甚至可以使离子之间带相反的电荷,再次增加了粒子之间的排斥作用,因此胶体得以再次稳定;混凝剂之间具有线性结构,具有能和颗粒表面发生化学反应的基团,形成的这些基团能够把颗粒与混凝剂高效的连接起来,混凝剂与胶体表面的作用主要是因为胶体表面与不带电的物质之间的范德华力而产生吸附架桥作用;卷扫作用主要是对混凝剂以而言的,这些混凝剂添加到废水中会发生水解,并生成沉淀,由于沉淀数量和表面积极大,因此之间会有孔网,而部分悬浮物会被吸附到孔网里面而得以去除。目前,广为应用的混凝剂主要有无机混凝剂、有机混凝剂、微生物以及符合混凝剂。
2.2 沿程SS浓度去除分析
装置运行稳定后各池子中SS浓度以及各池子中SS的去除率变化曲线见图2。
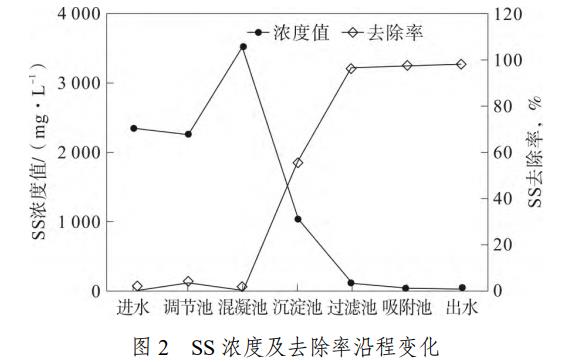
分析可知,进水中SS浓度值为2357.4mg・L-1,调节池中SS浓度值为2263.7mg・L-1、去除率为3.97%;混凝池中SS浓度值为3526.1mg・L-1,远大于进水中SS浓度;混凝池中SS浓度为3526.1mg・L-1、去除率为55.36%;沉淀池中SS浓度为1052.4mg・L-1、去除率为55.36%;过滤池中SS浓度为125.6mg・L-1、去除率为96.47%;吸附池中SS浓度为41.5mg・L-1、去除率为98.24%;出水中SS浓度为2263.7mg・L-1、去除率为98.41%。因进水水质和水量波动较大,调节池主要是调节水量和水质的,故废水流经调节池后SS浓度值几乎没有变化,只有一些粒径较大的悬浮物在池内运动过程中通过沉淀得以去除;在混凝池中由于添加了混凝剂和助凝剂,该物质投入水中后本身就会形成沉淀,颗粒物被吸附进入混凝剂形成的沉淀中,由于此时还来不及沉淀,故废水流经混凝池后SS浓度值升高明显,远大于进水中SS浓度值;废水流经沉淀池后在混凝池中形成的沉淀很快被沉淀下来,故此时SS浓度下降明显,去除率达到55.3%;一些细小粒径的SS由于重量不够在沉淀池无法沉淀,进入过滤池后这些SS被截留下来,故在过滤池中大部分SS被截留下来,SS浓度值又大大下降,从沉淀池至过滤池SS去除率增加了41.11%,吸附池主要是吸附少数过滤池中未过滤完全的极细小颗粒,故SS浓度变化不明显,从过滤池至吸附池SS去除率仅增加了1.77%。
2.3 Ca(OH)2添加量试验结果及分析
絮凝的作用主要是使一些胶体粒子或者较小的悬浮物凝聚,且主要是正对不溶于水的物质,由于煤矿废水中的Ca2+、Mg2+以及SO42-都是水溶性物质,故直接添加混凝剂作用效果不大,故应在混凝剂投入之前先添加适量的熟石灰(Ca(OH)2),Ca(OH)2可以和水中的Mg2+以及SO42-形成CaSO4和Mg(OH)2沉淀,废水中会产生一定量的CO2,该气体也可与Ca(OH)2可生成CaCO3沉淀,有了这些沉淀后会使SO42-的絮凝作用大大增强,故为探讨Ca(OH)2最适宜的添加量共进行两组试验(PAC和PAF试验),试验前先调节废水pH至7左右,保证实验室气温在25℃,每组试验又分为7小组,每小组用烧杯盛水1L,分别添加浓度为0、0.2、0.4、0.6、0.8、1.0、1.2g・L-1的Ca(OH)2,在7个PAC试验中各添加30mg・L-1的PAC,7个PAF试验中各添加30mg的PAF,控制搅拌速度约150r/min,搅拌约2min,开始絮凝时控制搅拌速度为20r/min,控制絮凝时间为10min,随后静止20min,取上清液测量水中总硬度以及SO42-含量,各物质含量及试验现象见表3,不同Ca(OH)2投加量下总硬度以及SO42-去除率曲线如图3和图4。
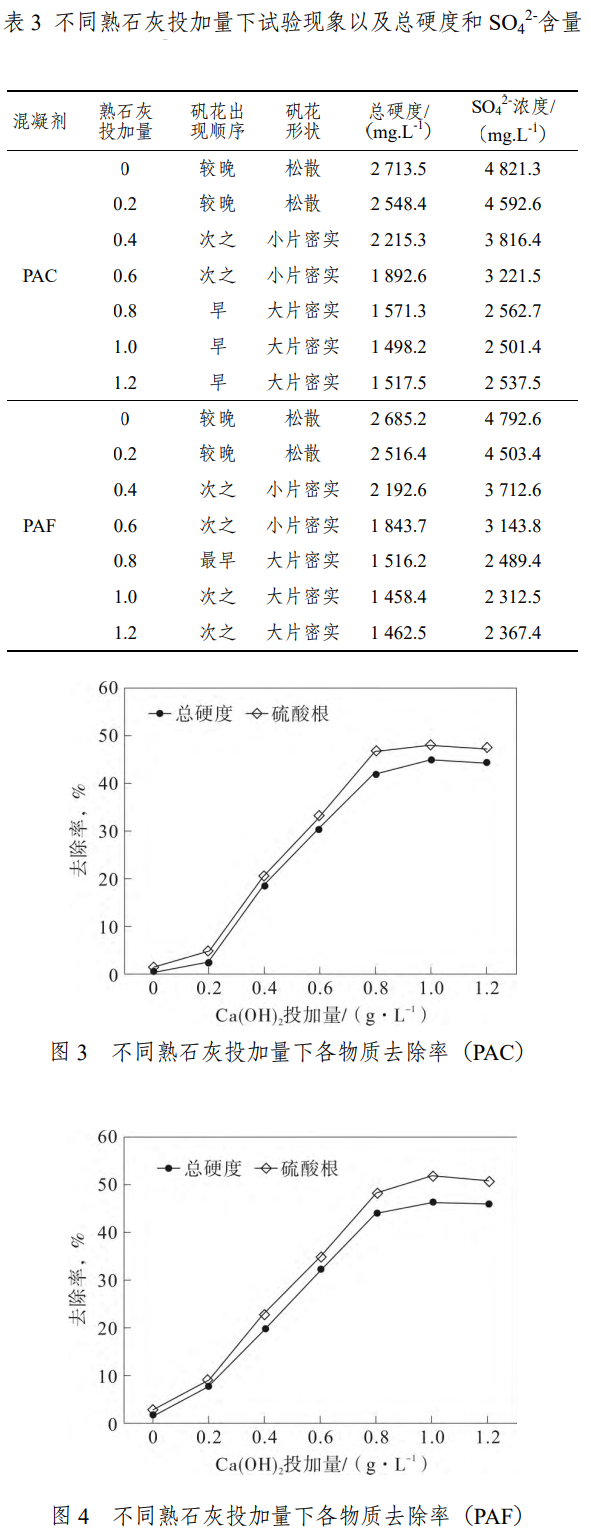
从图3分析可知:添加PAC混凝剂时,在不添加Ca(OH)2时,相比进水中浓度,混凝过程总硬度去除率为0.4%,SO42-去除率为1.37%;当添加浓度为0.2g・L-1的Ca(OH)2时,相比进水中浓度,混凝过程总硬度去除率为6.46%,SO42-去除率为4.66%;当添加浓度为0.4g・L-1的Ca(OH)2时,相比进水中浓度,混凝过程总硬度去除率为18.69%,SO42-去除率为20.78%;当添加浓度为0.6g・L-1的Ca(OH)2时,相比进水中浓度,混凝过程总硬度去除率为30.53%,SO42-去除率为33.13%;当添加浓度为0.8g・L-1的Ca(OH)2时,相比进水中浓度,混凝过程总硬度去除率为42.33%,SO42-去除率为46.8%;当添加浓度为1g・L-1的Ca(OH)2时,相比进水中浓度,混凝过程总硬度去除率为45.01%,SO42-去除率为48.07%;当添加浓度为1.2g・L-1的Ca(OH)2时,相比进水中浓度,混凝过程总硬度去除率为44.3%,SO42-去除率为47.33%。
从图4分析可知:添加PAF混凝剂时,在不添加Ca(OH)2时,相比进水中浓度,混凝过程总硬度去除率为1.44%,SO42-去除率为0.51%;当添加浓度为0.2g・L-1的Ca(OH)2时,相比进水中浓度,混凝过程总硬度去除率为7.64%,SO42-去除率为6.52%;当添加浓度为0.4g・L-1的Ca(OH)2时,相比进水中浓度,混凝过程总硬度去除率为19.52%,SO42-去除率为22.93%;当添加浓度为0.6g・L-1的Ca(OH)2时,相比进水中浓度,混凝过程总硬度去除率为32.33%,SO42-去除率为34.74%;当添加浓度为0.8g・L-1的Ca(OH)2时,相比进水中浓度,混凝过程总硬度去除率为44.35%,SO42-去除率为48.32%;当添加浓度为1g・L-1的Ca(OH)2时,相比进水中浓度,混凝过程总硬度去除率为46.67%,SO42-去除率为52.01%;当添加浓度为1.2g・L-1的Ca(OH)2时,相比进水中浓度,混凝过程总硬度去除率为46.32%,SO42-去除率为50.86%。
图3和图4均说明当不添加Ca(OH)2时,总硬度和SO42-几乎无去除,随着Ca(OH)2浓度的增加,两物质的去除率均呈逐渐增大,至Ca(OH)2浓度为1g・L-1时,上升趋势差不多停止,说明当Ca(OH)2浓度为1g・L-1时为最佳投药量。
2.4 混凝剂投加量试验结果与分析
上节中已得出Ca(OH)2最佳投药量为1g・L-1,故为保证单一变量,控制Ca(OH)2浓度为1g・L-1,改变PAC和PAF的用量,试验分为两组,一组添加PAC,另一组添加PAF,每组试验又分为7小组,每小组用烧杯盛水1L,第一组分别添加浓度为15、20、25、30、35、40、45mg・L-1的PAC,另一组分别添加浓度为15、20、25、30、35、40、45mg・L-1的PAF,控制搅拌速度约150r/min,搅拌约2min,开始絮凝时控制搅拌速度为20r/min,控制絮凝时间为10min,随后静止20min,取上清液测量水中总硬度以及SO42-含量,各物质含量及试验现象见表4,不同Ca(OH)2浓度为1g・L-1时不同PAC和PAF投加量下总硬度以及SO42-去除率曲线如图4和图5。
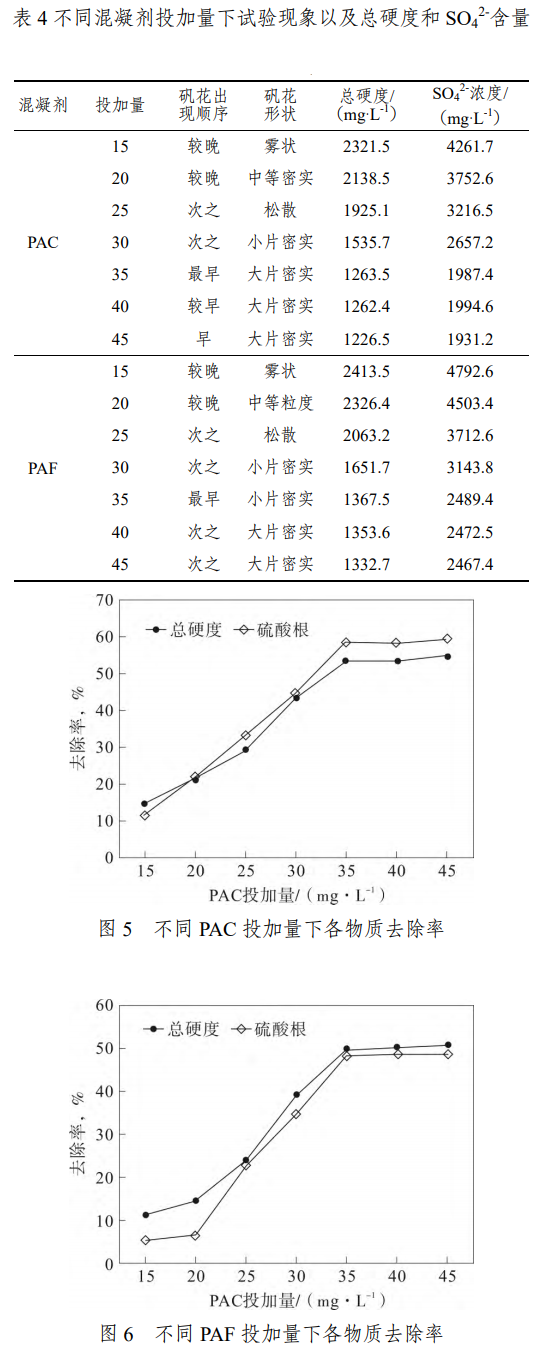
从图5分析可知:Ca(OH)2浓度为1g・L-1下,当添加PAC为15mg・L-1时,相比进水中浓度,混凝过程总硬度去除率为14.79%,SO42-去除率为11.53%;当添加浓度为20mg・L-1的PAC时,相比进水中浓度,混凝过程总硬度去除率为21.51%,SO42-去除率为22.1%;当添加浓度为25mg・L-1的PAC时,相比进水中浓度,混凝过程总硬度去除率为29.34%,SO42-去除率为33.26%;当添加浓度为30mg・L-1的PAC时,相比进水中浓度,混凝过程总硬度去除率为43.64%,SO42-去除率为44.85%;当添加浓度为35mg・L-1的PAC时,相比进水中浓度,混凝过程总硬度去除率为53.63%,SO42-去除率为58.75%;当添加浓度为40mg・L-1的PAC时,相比进水中浓度,混凝过程总硬度去除率为53.66%,SO42-去除率为58.59%;当添加浓度为45mg・L-1的PAC时,相比进水中浓度,混凝过程总硬度去除率为54.98%,SO42-去除率为59.91%。
从图6分析可知:Ca(OH)2浓度为1g・L-1下,当添加PAF为15mg・L-1时,相比进水中浓度,混凝过程总硬度去除率为11.43%,SO42-去除率为5.12%;当添加浓度为20mg・L-1的PAF时,相比进水中浓度,混凝过程总硬度去除率为14.61%,SO42-去除率为6.52%;当添加浓度为25mg・L-1的PAF时,相比进水中浓度,混凝过程总硬度去除率为24.28%,SO42-去除率为22.93%;当添加浓度为30mg・L-1的PAF时,相比进水中浓度,混凝过程总硬度去除率为39.36%,SO42-去除率为34.73%;当添加浓度为35mg・L-1的PAF时,相比进水中浓度,混凝过程总硬度去除率为49.81%,SO42-去除率为48.32%;当添加浓度为40mg・L-1的PAF时,相比进水中浓度,混凝过程总硬度去除率为50.32%,SO42-去除率为48.68%;当添加浓度为45mg・L-1的PAF时,相比进水中浓度,混凝过程总硬度去除率为51.08%,SO42-去除率为48.08%。
图5和图6均说明随着投加的PAC或PAF混凝剂浓度的增加,两物质的去除率均呈逐渐增大,至当PAC和PAF浓度均为35mg・L-1时,上升趋势差不多停止,说明当混凝剂浓度为35mg・L-1时为最佳投药量。
3、结语
本文以山西朔州怀仁矿区废水作为研究对象,采用自行设计的混凝工艺,研究了混凝工艺处理该矿区废水时需投加的最佳用量,结果表明:
(1)相比进水,SS浓度在调节池变化,经混凝池后SS浓度增大较多,SS的去除主要是在沉淀池和过滤池中,这两个反应池内SS的去除率分别为55.36和96.47%。
(2)当添加PAC或者PAF为混凝剂时,煤矿废水总硬度和SO42-的去除率随投加的Ca(OH)2浓度的增加而增大,当Ca(OH)2浓度为1g・L-1时为最佳投药量;
(3)随PAC和PAF浓度的增加,废水中总硬度和SO42-的去除率逐渐增大,当PAC和PAF投加量均为35mg・L-1时为最佳投药量。(来源:中国煤炭地质总局)
