铬及其化合物是地下水中常见的污染物,主要来源于冶金、电镀、金属加工、制革、油漆、印染和木材防腐等行业生产、贮存、运输、经营、使用和处置等过程中产生的含铬废水、废气和废渣。铬在地下水环境中主要以Cr(Ⅲ)和Cr(Ⅵ)的形式存在,Cr(Ⅵ)的化合物具有潜在致癌形态,并且由于Cr(Ⅵ)溶解度高、表面带负电,其在地下水中极易迁移。而Cr(Ⅲ)的迁移性差并且毒性低,它通常以氧化物和氢氧化物形式沉淀。
目前,关于Cr(Ⅵ)污染地下水的修复方法主要有化学还原法、电动修复和生物修复方法等。其中零价铁渗透反应格栅(zero-valent iron Permeable reactive barrier,Fe0 -PRB)技术以其处理费用低、使用寿命长、能有效截获地下水污染羽状体等特点,被广泛地用于Cr(Ⅵ)污染地下水的原位修复。Fe0 -PRB的长期运行性能受到污染场地地下水成分的影响 。
氮肥、动物粪便和农药的超量施用,使得硝酸根(NO3- )成为地下水中普遍存在的污染物之一。在很多情况下,NO3- 与Cr(Ⅵ)成为共存污染物。冯爱云等[17] 的柱实验研究认为NO3- 促进零价铁(Fe0 )去除Cr(Ⅵ),原因可能是由于颗粒铁由水腐蚀产物Fe3 O4 转换为高价铁氧化物时释放出的酸的作用。RIVERO-HUGUET 等的批实验研究指出NO3- 的存在对Fe0 去除Cr(Ⅵ)的影响随pH 变化,pH = 2NO3- 提高Fe0 去除Cr(Ⅵ)的反应速率,而当pH = 6 时,NO3- 的存在对Fe0 去除Cr(Ⅵ)的反应速率无影响。而孟凡生等 利用柱实验研究证明NO3- 对Fe0 去除Cr(Ⅵ)无影响。
本研究利用批实验和柱模拟实验,全面而透彻地对比分析了存在NO3- 和不存在NO3-3 情况下零价铁对Cr(Ⅵ)的去除差异性,分析了NO3- 对Fe0 去除Cr(Ⅵ)的影响作用;通过长期运行连续流动的Fe0 柱模拟实验,研究了NO3- 对Fe0 -PRB 去除Cr(Ⅵ)的长效性影响。为实际场地进行地下水NO3- 和Cr(Ⅵ)复合污染的Fe0 -PRB 修复提供参数。
1 实验部分
1. 1 实验材料
铁屑(ETI-CC-1004,Connelly-GPM Inc. ,U. S. ):铁含量、粒径、比表面积、密度分别为96. 28% 、0. 25 ~2. 0 mm、1. 8 m2 ・g - 1 、和6. 43 g・cm - 3 ,筛分数为20 ~ 40 目。石英砂:粒径0. 5 ~ 1 mm,粗砂粒径1 mm,细沙粒径0. 5 mm。活性炭:粒径0. 5 mm。
Cr(Ⅵ)储备液:将2. 829 g 干燥的K2 Cr2 O7 溶于1 L 去离子水中,配成1 000 mg・L - 1 的标准储备液,放到棕色试剂瓶避光保存于4 ℃ 的冰箱中。
批实验和柱实验中所配污染溶液均在配制完成后通氮气驱氧0. 5 h,以保证实验在厌氧条件下进行。
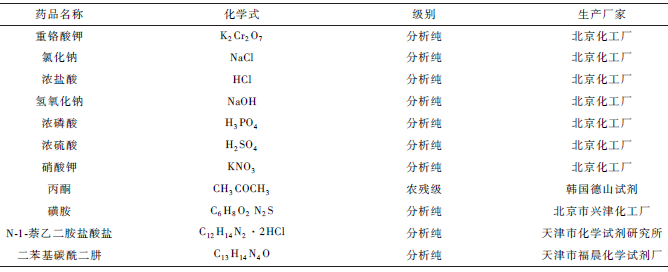
实验所用化学试剂详见表1。
表1 化学试剂
1. 2 实验方法
1. 2. 1 批实验方法
分别设计Cr(Ⅵ) + Fe 反应体系(简称CF 体系)和Cr(Ⅵ) + Fe + NO3- (简称CFN 体系)2 个反应体系,溶液均为50 mL,背景电解质为0. 01 mol・ L - 1 的NaCl,铁屑量为1 g(20 g・L - 1 ),Cr(Ⅵ) 浓度为10 mg・L - 1 ,NO3- -N 浓度为50 mg・L - 1 ,两个体系分别在不同的初始pH(5、7、9) 条件下反应,在室温(24 ± 0. 5)℃ 下,以175 r・min - 1 的速度在摇床进行震荡,于5、10、15、20、30、40、50 和60 min 时取样,过0. 45 μm 滤膜,测定pH 值、Cr(Ⅵ)和NO3- 、NO2- 和NH4+ 的浓度。所有实验均设置2 个平行样。
1. 2. 2 柱实验方法
柱实验采用内径4 cm,长15 cm 的2 个有机玻璃柱(见图1) 依次表示为L1、L2,具体参数如表2。柱子下端和上端均填有1. 5 cm 和1 cm 厚的粗砂和细沙,起到过滤、缓冲、保护的作用;中间部分是以铁屑为主的反应介质,孔隙体积约为80 mL,渗透流速均约为0. 9 ~ 1 m・d - 1 ,每个柱子在柱侧壁距柱下端2. 5、5、7. 5、10 和12. 5 cm 处设置5 个取样孔,分别记为孔1 ~ 5,对应的停留时间分别为0、0. 67、1. 33、2和2. 67 h。
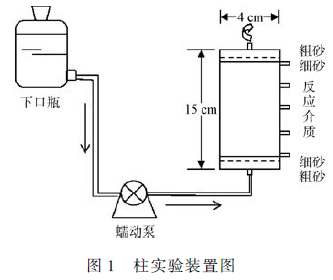
表2 柱子参数

L1 通入20 mg・L - 1 Cr(Ⅵ) 溶液,L2 通入20mg・L - 1 Cr(Ⅵ) + 100 mg・L - 1 NO3- -N 的混合溶液。溶液由柱子的下部输入上部流出,每隔一定孔隙体积数(PV)从上到下由取样孔依次取水样5 ~ 10 mL,过0. 45 μm 滤膜后测溶液的pH 值、Cr(Ⅵ)和NO3- 、NO2- 和NH4+ 浓度。实验柱子参数见表2。
1. 2. 3 测试方法
Cr(Ⅵ)、NO3- 和NO2- 均用紫外-可见分光光度计(spectrophotometers:Shimadzu,UV-1800) 测定,吸收波长分别为540 nm、220 和275 nm、540 nm。NH4+ 用离子色谱仪(Thermo Fisher,DIONEX ICS-900)测定。
pH 值由pH 测定仪(Sartourius,PB-10)获得。
2 结果与讨论
2. 1 硝酸盐对铁屑去除Cr( Ⅵ) 的影响批实验研究
2. 1. 1 硝酸盐对铁屑去除Cr( Ⅵ) 的影响
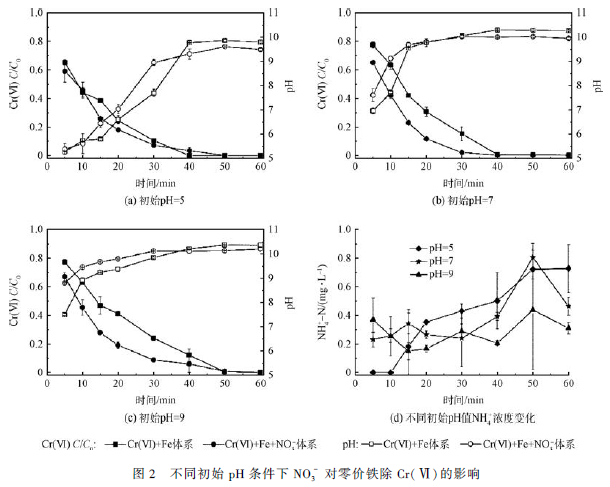
在初始pH 值分别为5、7 和9 的条件下,将50 mg・L - 1 的NO3- -N 溶液与10 mg・L - 1 的Cr(Ⅵ)溶液混合再加入铁屑建立CFN 体系,与铁屑单独去除Cr(Ⅵ)的CF 体系对比研究。结果如图2。(C 为溶液中Cr(Ⅵ)浓度,C0 为溶液初始Cr(Ⅵ)浓度)初始pH 为5 时(见图2(a)),CFN 体系中,5 min 后Cr(Ⅵ)的去除率为41% ,50 min 时Cr(Ⅵ)的浓度低于检出限;CF 体系中,5 min 后Cr(Ⅵ)的去除率为35% ,40 min 时Cr(Ⅵ)的浓度低于检出限。NO3- 促进了铁屑对Cr(Ⅵ)的去除。初始pH 为7 和9 时(见图2(b)和(c),NO3- 的促进作用更为明显。反应过程中,pH 逐渐升高,直至Cr(Ⅵ) 的浓度低于检出限,pH 保持不变,且有少量NO3- 被铁屑还原为NH4+ (见图2(d)),不同初始pH 值条件下生成的NH4+ 相差不大,NO2- 的浓度低于检出限。
与CF 体系相比,无论酸性(pH = 5)、中性(pH = 7) 或碱性(pH = 9) 条件下,NO3- 均促进Cr(Ⅵ) 的去除。
2. 1. 2 硝酸盐存在时铁屑去除Cr( Ⅵ) 的动力学拟合
将上述实验结果进行动力学拟合,如图3 所示。拟合得到反应速率常数k 和R2 见表3。
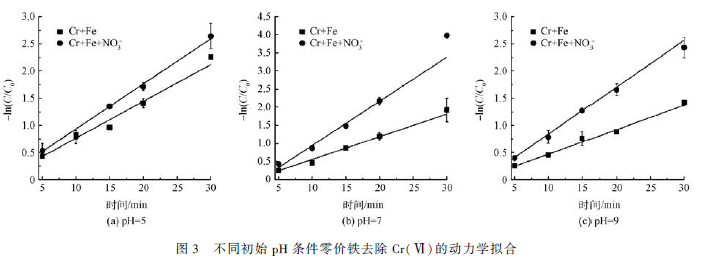
表3 不同pH 下NO3- 与反应速率常数关系
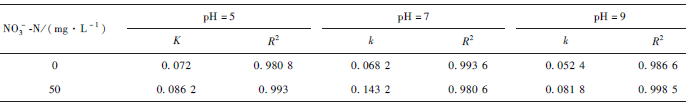
由表3 可知,当初始pH 为5 时CFN 体系和CF 体系k 值分别为0. 086 2 和0. 072 min - 1 ,pH 为7 时k值分别为0. 143 2 min - 1 和0. 068 2 min - 1 ,pH 为9 时k 值分别为0. 081 8 min - 1 和0. 052 4 min - 1 。不同初始pH 条件下,NO3- 的加入均使得铁屑去除Cr(Ⅵ)的速率升高,初始pH = 7 条件下促进作用最强,达到无NO3- 条件下反应速率的2. 1 倍。
2. 2 硝酸盐对铁屑去除Cr( Ⅵ) 的影响柱实验研究
柱实验在2 个有机玻璃柱中进行。L1 为控制柱通入Cr(Ⅵ)溶液,L2 通入Cr(Ⅵ) + NO3- 的混合溶液。采用铁屑作为主要反应介质,为了防止铁屑结块,将铁屑与石英砂进行混合。PV 是孔隙体积,1PV = 80 mL。在柱实验中,PV 常用作时间单位,即1PV 等同于80 mL 溶液通过实验柱所需的时间。
2. 2. 1 铁屑柱对Cr( Ⅵ) 的去除效果及NO3- 的还原
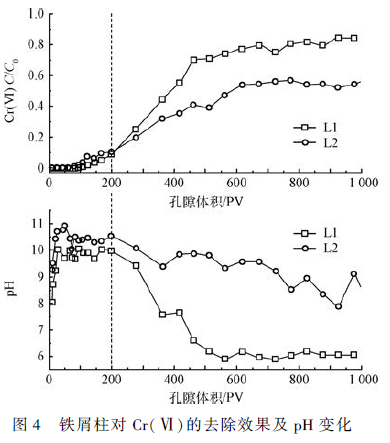
2 个柱子运行结果如图4 所示(C 为出水Cr(Ⅵ)浓度,C0 为进水Cr(Ⅵ)浓度)。于72 PV 时,L2 的出水Cr(Ⅵ)最先检出,L1 在93 PV 时Cr(Ⅵ)也开始被检出。198 PV 之前L2 对Cr(Ⅵ)的去除效果比L1差,运行初期NO3- 对铁屑去除Cr(Ⅵ)的反应有一定的抑制作用。198 PV 之后,L1 出水Cr(Ⅵ)浓度一直高于L2,说明NO3- 对铁屑去除Cr(Ⅵ)的反应有促进作用。
在开始通入污染溶液后,2 个柱子内的pH 均迅速增大。对于L1,在Cr(Ⅵ)开始穿透时,其出水pH也开始下降,198 PV 之后,pH 迅速下降。从化学计量学上分析(式(1)),1 mol 的重铬酸根(Cr2 O7^2 - ) 被Fe0 还原,会分别生成2 mol 的Cr3 + 和2 mol 的Fe3 + 以及14 mol 的OH - 。然而把生成的Cr3 + 和Fe3 + 完全沉淀只需12 mol 的OH - ,剩余的2 mol OH - 积累下来使得pH 升高。另外,Cr(Ⅵ)的还原速率快于生成的Cr(Ⅲ)沉淀速率,Fe0 的腐蚀也会增加溶液中OH - 的量[20] 。198 PV 后,L1 出水pH 迅速下降,这是由于L1 中的Fe0 开始出现部分钝化,失去了钝化膜并抑制了Fe0 对Cr(Ⅵ)的还原,Cr(Ⅵ)还原和OH - 的产生速率都开始下降。而563 PV 之后恢复到入水pH值,是由于大部分Fe0 钝化,只有少量的OH - 的产生,而金属离子的沉淀却仍在进行,OH - 消耗,溶液pH 下降。
Cr2 O7 + 2Feo + 7H2 O↔2Cr2 + + 2Fe3 + + 14OH - (1)
而对于L2,其体系内的pH 变化滞后于L1,特别是198 PV 之后,L1 和L2 的出水pH 差异明显。L1的出水pH 值迅速下降,300 PV 时,就已经达到9 以下,而L2 直到725 PV 之前出水pH 一直大于9,之后的出水pH 也一直维持在8 以上,而L1 却在563 PV之后恢复到入水pH 值6 左右。2 个柱子中的pH 差异明显,一方面是由于L2 中与Cr(Ⅵ) 同时通入的NO3- 与Fe0 反应过程中消耗H + ,可以增大pH值;另外一方面原因可能是由于NO3- 与Fe0 反应过程生成的副产物磁铁矿(Fe3 O4 )。以往的研究证明Fe3 O4 具有阻滞反应产物在Fe0 表面堆积和促进电子传导作用 ,从而促进了Fe0 对Cr(Ⅵ)的还原,进一步增大了L2 体系的pH 值。除此之外,虽然Fe3 O4 基本不与NO3- 发生氧化还原反应 ,但是Fe3 O4 却可以将Cr(Ⅵ)还原,一定程度上促进了Cr(Ⅵ)的去除。
2. 2. 2 铁屑去除Cr( Ⅵ) 的动力学拟合
为了更好地研究铁屑柱对Cr(Ⅵ)的去除效果的稳定性,分别对2 个柱子不同孔隙体积时的Cr(Ⅵ)的浓度变化进行研究,并进行动力学拟合,结果如图5 所示。
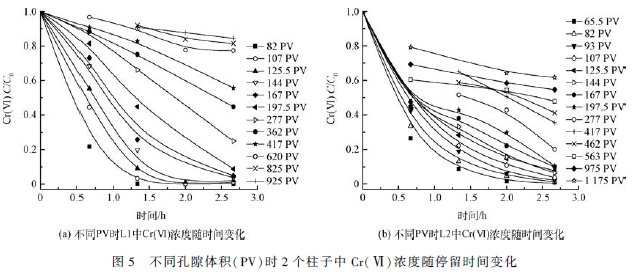
表4 两个柱子不同孔隙体积时的半衰期( t1 / 2 )
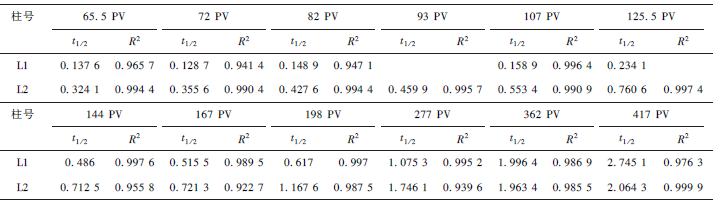
观察2 个柱子不同孔隙体积时Cr(Ⅵ)浓度随停留时间变化(见图5),整个运行过程L1 中Cr(Ⅵ)浓度随停留时间的变化符合准一级动力学(见图5(a)),L2 在198 PV 之前符合准一级动力学,198 ~ 618PV、925 ~ 1 175 PV 符合零级动力学(见图5(b))。拟合得到的半衰期值(t1 / 2 )如表4 所示。运行初期,L1的t1 / 2 小于L2,L1 对Cr(Ⅵ)的还原反应速率更快;随着反应的进行,两个柱子的t1 / 2 均逐渐增大,198 ~ 277PV 时,t1 / 2 迅速增大,反应速率变小;但362 PV 时,L1 的t1 / 2 开始大于L2 的,L2 体系中的Cr(Ⅵ)的还原反应速率开始超过L1。
2. 2. 3 NO3- 对铁屑柱去除Cr( Ⅵ) 的影响
为了进一步探讨NO3- 的影响机理,把L2 作为研究对象,对比L1 和L2 不同孔隙体积间的Cr(Ⅵ)浓度变化。
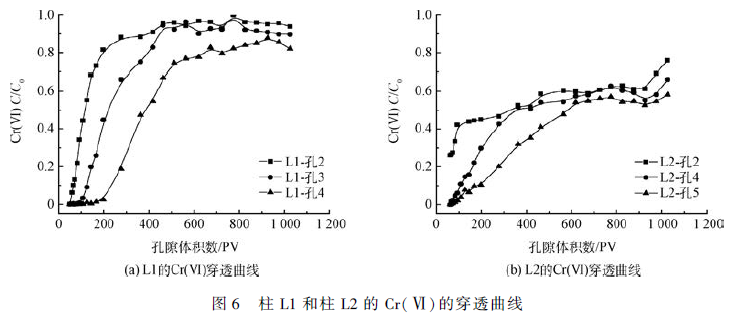
图6 表明,L1 出水Cr(Ⅵ)有检出后,出水Cr(Ⅵ)浓度随着孔隙体积数的增加而升高。实验前期Cr(Ⅵ)浓度升高较快,当Cr(Ⅵ)去除率为20% 左右时,Cr(Ⅵ)浓度的升高趋于平稳。整个时期各孔间的浓度都相差较大,表现为柱子逐段被钝化。L2 中出水Cr(Ⅵ)浓度随着孔隙体积数的增加也同样增大,与L1不同的是,对Cr(Ⅵ)的去除率为50% 左右时,Cr(Ⅵ)浓度的升高趋于平稳,且各孔间的浓度差逐渐减小,表现为铁屑柱整体性的同步钝化。具体参见污水宝商城资料或http://www.dowater.com更多相关技术文档。
3 结论
1)批实验结果表明在不同初始pH 条件下(pH = 5(酸性)、pH = 7(中性)、pH = 9(碱性)),NO3- 的加入均使得铁屑去除Cr(Ⅵ)的速率升高,初始pH = 7 条件下促进作用最强,达到无NO3- 条件下反应速率的2. 1 倍。
2)柱实验证明NO3- 的存在将Fe0 柱对Cr(Ⅵ)的去除分为3 个反应阶段:高效期( < 198 PV),快速钝化-平稳钝化期(198 ~ 1 025 PV),彻底钝化期( > 1 025 PV)。其中在高效期,NO3- 表现为对Fe0 反应位点的竞争,抑制Cr(Ⅵ)还原。后面的2 个阶段,NO3- 则呈现明显的促进作用。整体而言,NO3- 的存在促进了Fe0 柱对Cr(Ⅵ)的还原,增强了Fe0 柱除Cr(Ⅵ)的长效性,提高了Fe0 柱对Cr(Ⅵ)的去除效率。
3)NO3- 促进Fe0 对Cr(Ⅵ)还原的机制是由于NO3- 与零价铁反应的副产物为Fe3 O4 ,而Fe3 O4 不仅可以将Cr(Ⅵ)还原,而且具有阻滞反应产物在Fe0 表面堆积和促进电子传导的作用。