申请日2013.01.29
公开(公告)日2013.05.22
IPC分类号C02F9/06
摘要
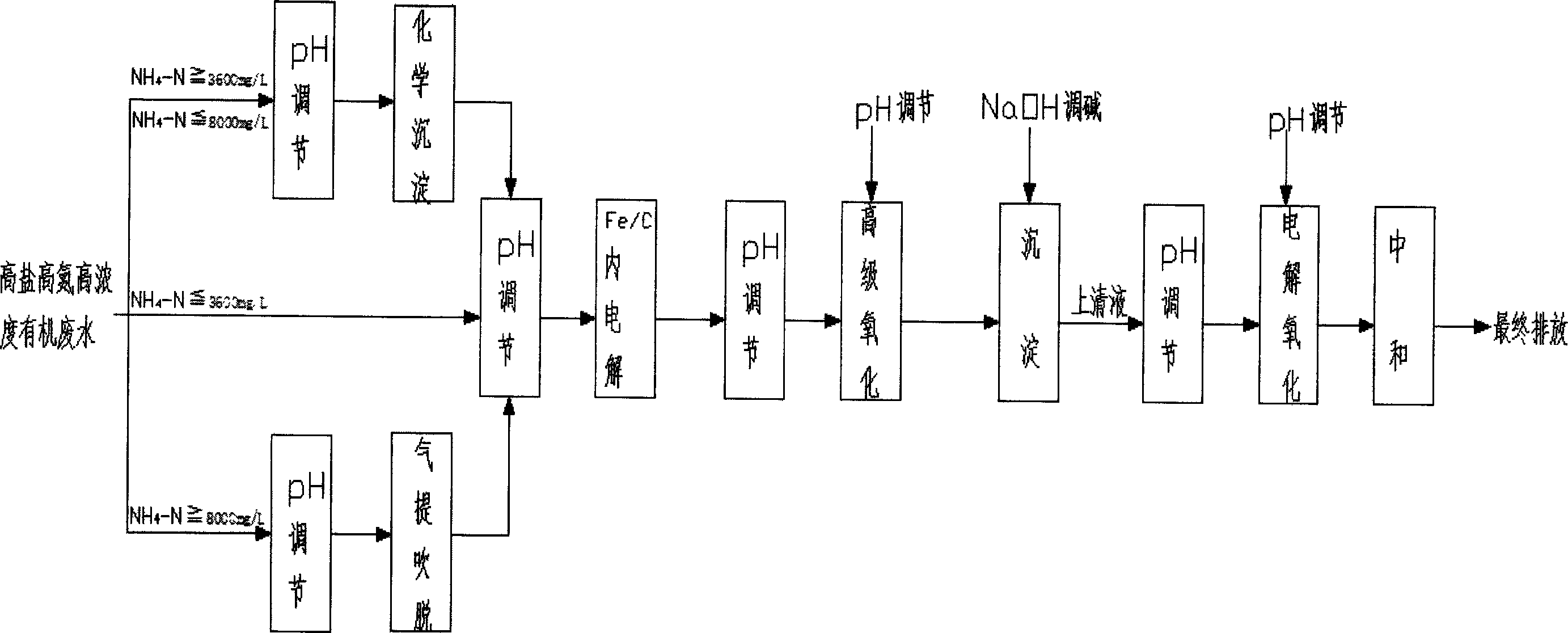
本发明公开了一种针对高盐高氮高浓度有机废水的处理方法,本发明根据废水水质,采用三段式处理工艺。A段加入铁屑和含碳颗粒,在曝气条件下反应分解40~50%的有机物;B通低压直流电,同时滴加H2O2,可以分解70~80%的有机污染物;C段提高电压,减少H2O2滴加量,彻底分解有机物,并产生大量化合性氯去除氨和氮化物。若原废水氨氮浓度过高,增加吹脱或化学沉淀的预处理脱氮过程。本发明处理高盐高氮高浓度有机废水的方法,可控性强,适用范围广。在保证高效处理的前提下,控制电耗成本,具有一定的实用价值。
权利要求书
1.一种高盐高氮高浓度有机废水的处理方法,其特征在于:所述的一 种高盐高氮高浓度有机废水,盐度≥6%,若氨氮浓度≤3600mg/L,可直 接用本方法处理后达标排放,若氨氮浓度为3600~8000mg/L时,用化学 沉淀的方法进行预处理脱氮;若氨氮浓度≥8000mg/L,采用氨气提吹脱 的方法进行预处理脱氮。
2.如权利要求书1所述的处理方法,其特征在于:当所述的高盐高氮 高浓度有机物废水的氨氮浓度≤3600mg/L时,该方法按照以下几个步骤 进行:
(1)调节上述废水的pH为3~4;
(2)在上述废水中加入Fe/C=4~5∶1的铁屑和含碳颗粒,在曝气的条 件下,停留时间为4~5h,可分解废水中40~50%的有机物,完成废水的A 段初步处理;
(3)调节上述废水的pH为2~3.5;
(4)对上述废水外加5~10V的直流电压,通电时间为4.5~6h,并 在反应过程中滴加浓度为30%的H2O2,滴加量为0.5~0.8ml/gCOD,以此 分解废水中70~80%的有机污染物,完成B段的废水处理;
(5)调节上述废水的pH为8~9,自然沉降3~4h后,上清液进入后 续反应工艺;
(6)调节上清液的废水的pH为4~6;
(7)提高步骤(4)中的电压为20~25V,通电时间为0.5~2h,将上 述处理过的废水进一步电化学氧化,同时浓度为30%的H2O2的滴加量为 0.05~0.1ml/gCOD,彻底分解有机物,并产生大量化合性氯去除氨和氮化 物,实现废水C段处理;
(8)中和上述废水的pH为中性,实现废水的最终处理排放。
3.根据权利要求书2所述的处理方法,其特征在于:所述的步骤(2) 中的电流密度为50~100mA/cm2,两极板的间距为5~17cm;所述的步骤 (4)中的电流密度为200~400mA/cm2,两极板的间距为5~11cm。
4.根据权利要求书2所述的处理方法,其特征在于:所述的步骤(2) 中双氧水采用间歇的方法滴加,每一次滴加双氧水用量的20%~40%,待 前次滴加双氧水产生的气泡速率稳定后,再滴加余下的双氧水。
5.根据权利要求书2所述的处理方法,其特征在于:在所述的步骤(4)、 (7)的反应进行过程中,需要不定时调节pH值,使之维持在该步骤的初 始水平。
6.根据权利要求书2所述的处理方法,其特征在于:所述的步骤(2) 中铁屑为铸铁或碳钢,含碳颗粒可用活性炭、焦炭、无烟煤。所述的步骤 (4)、(7)中电化学氧化所用的阴、阳极材料均为石墨。
7.根据权利要求书2所述的处理方法,其特征在于:所述的步骤(7) 中每0.5~1h改变直流电的流向一次。
8.根据权利要求书1所述的处理方法,其特征在于:所述的盐度≥6% 的高盐高氮高浓度有机废水,其中的氯离子与氨氮(以N计)的摩尔比≥ 4∶1。
9.根据权利要求书1所述的处理方法,其特征在于:所述的高盐高氮 高浓度有机废水中,当氨氮浓度为3600~8000mg/L时,调节pH为8~9, 滴加MgO和Na2HPO4・12H2O为沉淀剂去除氨氮,n(Mg2+)∶n(NH4+)∶ n(PO43-)=1.15~1.4∶1∶0.8~1.2;当氨氮浓度≥8000mg/L,调节pH为10.5~11, 采用氨气提吹脱的方法,气液体积比为3000~3600∶1,去除氨氮。
说明书
一种高盐高氮高浓度有机废水的处理方法
技术领域
本发明涉及废水处理领域,尤其涉及一种化工的高盐高氮高浓度有机 废水的处理方法。
背景技术
随着工业的快速发展,印染、造纸、化工、制药、石油以及发酵等部 门在生产大量产品的同时也不可避免地产生了高盐高氮高浓度有机物废 水,这类废水的特点是含盐量高,总含盐(如Na、K、Cl-、S042-等)质量 分数≥4%,还含有有机物和质量分数≥3.5%的总溶解性固体物(TDS)。 这些废水若未经处理直接排放,势必会对水体生物、生活饮用水和工农业 生产用水产生极大的危害。
传统的废水处理方法是采用生化处理工艺,但是高盐废水的高盐度环 境会抑制微生物的生长,破坏微生物的细胞膜和菌体的酶,由此导致微生 物去除率降低,增加生物处理的难度。而仅仅采用化学法、物理法处理工 艺则难以实现COD等达标排放,且处理成本较高。随着研究的不断深入, 提出了光催化氧化、电化学氧化法、fenton等高级氧化技术,这些方法具 有高效性、普遍性和彻底性的特点,但是存在处理成本高、反应条件不成 熟等局限,目前应用尚未广泛。
专利ZL201210017318.1公开了一种冶金工业高盐废水的处理方法,该 发明专利首先使用低压直流电源,将高盐废水进行电解,将水中油、悬浮 物、重金属离子的含量处理到微量,然后用化学法对电解液进行化学处理, 使高盐废水中的COD、总磷含量达到国家一级排放标准,该方法具有处理 时间短,工艺简单,成本低的优点,但是其所使用的技术的电流效率不高, 且处理的高盐废水的COD含量较低,所以该法不适用COD>10000mg/L的 高盐高浓度有机废水的处理,并且该法也不具备去除氨氮的功能。
综上所述,目前还没有一个成熟并且经济有效的技术可用于高盐高氮 高浓度有机废水的处理,所以亟需改进现有技术或开发一种新的技术方案 来解决当前这类废水带来的水环境污染问题。
发明内容
针对现有高盐高氮高浓度有机废水处理技术的不足,本发明了公开了 一种盐度≥6%的高盐高氮高浓度有机废水的处理方法。
当该高盐废水中氨氮浓度≤3600mg/L,可直接用本方法处理后达标 排放,本方法按照以下几个步骤进行:
(1)调节上述废水的pH为3~4;
(2)在上述废水中加入Fe/C=4~5∶1的铁屑和含碳颗粒,在曝气 的条件下,停留时间为4~5h,可分解废水中40~50%的有机物,完成废 水的A段初步处理;
(3)调节上述废水的pH为2~3.5;
(4)对上述废水外加5~10V的直流电压,通电时间为4.5~6h, 并在反应过程中滴加浓度为30%的H2O2,滴加量为0.5~0.8ml/gCOD,以 此分解废水中70~80%的有机污染物,完成B段的废水处理;
(5)调节上述废水的pH为8~9,自然沉降3~4h后,上清液进 入后续反应工艺;
(6)调节上清液的废水的pH为4~6;
(7)提高步骤(4)中的电压为20~25V,通电时间为0.5~2h, 将上述处理过的废水进一步电化学氧化,同时浓度为30%的H2O2的滴加 量为0.05~0.1ml/gCOD,彻底分解有机物,并产生大量化合性氯去除氨和 氮化物,实现废水C段处理;
(8)中和上述废水的pH为中性,实现废水的最终处理排放。
所述的步骤(1)中首先调节废水的pH为3~4,因为pH值直接影响铁 屑对废水的处理效果,过低的pH值会改变产物的存在形式,影响效率,而 pH值在中性或碱性条件,反应基本不反应。
所述的步骤(2)中铁屑和周围的含碳颗粒形成了宏观电池:
Fe作为阳极:Fe-2e→Fe2+
C作为阴极:2H++2e→2H→H2
而有O2时,还会发生如下反应:
O2+4H++2e→2H2O
O2+2H2O+4e→4OH-
2Fe2++O2+4H+→2H2O+Fe3+
电极反应生成的活性物质能够和水中的有机物发生氧化还原反应,从 而达到去除污染物的目的。并且,随着反应的进行,废水的pH值会有所升 高,对该废水进行曝气,当有O2存在的条件下,Fe2+、Fe3+会生成Fe(OH)2和Fe(OH)3絮凝沉淀,可吸附凝聚废水中的悬浮污染物。曝气还可以防止 铁屑结块,并利用摩擦去除铁屑表面钝化形成的膜,提高反应效率。设定 Fe/C=4~5∶1,停留时间为4~5h,若C量过低,则反应不充分,效率不高, C量过高,则Fe、C电极表面失去平衡,处理效果变差。而停留时间过长, 不仅增加铁的用量,而且Fe2+大量转化为Fe3+,不利于后续工艺对Fe2+的使 用。
所述的步骤(2)可分解废水中40~50%的有机污染物,完成废水的A 段初步处理。
所述的步骤(3)中调节废水的pH为2~3.5,这是因为步骤(2)中反应剩 余的Fe2+和步骤(4)中滴加的H2O2在酸性的条件下可以发生链式反应,催 化生成羟基自由基(・OH),而・OH具有很高的电负性或亲电性,能加 快有机物和还原性物质的氧化,高效率分解废水中的有机物。
所述的步骤(4)中的电流密度为50~100mA/cm2,两极板的间距为 5~17cm,废水盐度≥6%,由以下①②③公式可知,
盐度y=1.3888*x-0.02478*x*t-6171.9,x为电导率,t为水温; ①
R=L/(x*s),L为极板间距,s为电极间有效面积; ②
R=U/I,U为极板间电压,I为电流; ③
两极板间的电压为5~10V。设置A段反应的通电时间为4.5~6h,浓 度为30%的H2O2的滴加量为0.5~0.8ml/gCOD,一般说来,电压越高, 电流密度越大,通电时间越长,试剂的投加量越大,都可以促进有机物分 解效率的提高,但是电压越高,电流密度越大,通电时间越长也就使得电 耗更多,会带来更高的经济成本,而试剂投加越多,也会增加运行的成本, 所以采用这些参数,使电解和试剂氧化的组合作用达到一个最佳效果。其 中,双氧水采用间歇的方法滴加,每一次滴加双氧水用量的20%~40%, 待前次滴加双氧水产生的气泡速率稳定后,再滴加余下的双氧水。这是因 为如果H2O2一次性滴加量过大,它分解产生的羟基自由基・OH的消耗速 率远远大于其产生速率,多余的・OH转而消耗还未分解的H2O2,造成试 剂的浪费和处理成本的升高。
所述的步骤(4)可分解废水中70~80%的有机污染物,完成废水的初 步处理。
所述的步骤(5)调节上述废水的pH为8~9,自然沉降3~4h,这是因 为水中多余的Fe2+、Fe3+对后续电氧化的干扰非常大,这一步骤可以使其 转化为Fe(OH)2和Fe(OH)3沉淀,并通过沉降的方法去除。
所述的步骤(6)中调节pH为4~6,当pH不在这个范围内时,H2O2的分解速率会明显加快。
由上述步骤(4)中的计算方法可得,所述的步骤(7)中设置电流密 度为200~400mA/cm2,两极板的间距为5~11cm时,所使用的直流电压 20~25V,通电时间为0.5~2h。同时,浓度为30%的H2O2的滴加量为 0.05~0.1ml/gCOD,以提高电压的方法来彻底分解废水中残留的有机物, H2O2的少量滴加提高了电流效率,减少了反应时间,节约电耗成本。
所述的步骤(7)中电化学氧化所用的阳极、阴极材料均为石墨,实 验中发现,在以SnO2/Ti或PbO2/Ti为电极的电化学氧化过程中,电极被 严重腐蚀,损耗很厉害,这样带来的结果就是增加了电极更换的频率,提 高了运行成本,且降低废水处理效果。而石墨是一种较为常见的经济的材 料,且阴、阳极材料一致的情况下,可0.5~1h改变直流电的流向一次, 这不会影响废水的处理效果,却可以平衡阴、阳电极之间的损耗,最大化 延长电极的使用寿命。
所述的步骤(4)和所述的步骤(7)在反应进行过程中,需要不定时 调节pH值,使之维持在一个稳定的酸碱环境中,保证反应的高效进行。
一种可直接用本方法达标处理的盐度≥6%的高盐高氮高浓度有机废 水,其中的氯离子与氨氮(以N计)的摩尔比≥4∶1,这是因为高盐废水在 电解条件下,在阳极上,氯离子氧化成为氯原子,进而产生氯气,进入水 中生成HClO,与水中的氨或氮化物反应,使之生成N2去除,这就免去了 折点加氯法中外加液氯的昂贵费用及高要求的保存条件,经济安全,当水 中氯离子与氨氮(以N计)的质量比≥10∶1时,可保证水中的氨氮在折点 被完全去除,达到排放标准的要求。可是对于中高浓度的氨氮废水,废水 中本身含有的氯量不能达到氨氮达标处理的需要,需要外加氯气或次氯酸 钠,这不仅需要考虑存储问题,而且带来了余氯消除的问题,增加了处理 成本,所以,若其中的氨氮浓度≥3600mg/L时,先采用适当的预处理手 段降低氨氮浓度后,再使用本方法达标处理。当氨氮浓度为3600~8000 mg/L时,调节pH为8~9,滴加MgO和Na2HPO4・12H2O为沉淀剂进行预处理 脱氮,n(Mg2+)∶n(NH4+)∶n(PO43-)=1.15~1.4∶1∶0.8~1.2。当氨氮浓度≥ 8000mg/L时调节pH为10.5~11,采用氨气提吹脱的方法,气液体积比为 3000~3600∶1,进行预处理脱氮。化学沉淀法处理速度快,效率高,但是 药剂的添加成本高,所以将它用于中低浓度氨氮的预处理,氨气体吹脱运 行费用低,流程简单,适应于高氨氮的废水,但是对于高浓度氨氮废水, 其处理效率达到90%,出水氨氮值仍然较高,需要后续处理才能达标,所 以氨气体吹脱也不能作为单独的氨氮处理手段。
本发明针对传统生化法不能处理的高盐高氮高浓度有机废水,提出了 一种三段式的处理工艺,电流效率较高,可控性强,可高效去除废水中高 含量的有机物和氨及氮化物,在此前提下,可控制电耗成本,具有工程实 用的潜能。