随着微生物学在污水处理领域的深化,反硝化聚磷菌(DPAOs)的发现颠覆了人们对传统生物脱氮除磷的认识。反硝化除磷的实现使得COD消耗量节省50%,吸磷过程由缺氧代替好氧,节省30%曝气量,相应的污泥产量减少50%,同时释放的CO2降低20%左右。基于反硝化除磷的理念,新型双污泥工艺——A2/O-移动床生物膜反应器(MBBR)应运而生。它具有处理流程简单,运行管理方便,脱氮除磷效果稳定等诸多优点,可实现低碳氮比(C/N)污水的深度脱氮除磷和节能降耗,应用前景较好。反硝化除磷工艺的改进和优化,使得传统污水处理工艺朝着高效率、低能耗的可持续方向发展。
反硝化除隣过程DPAOs对磷的吸收依赖于电子受体(NO3−-N或NO2−-N),MERZOUKI等研究表明,反硝化除磷效率很大程度上取决于电子受体的类型和浓度,然而由于反硝化除磷体系和运行条件的不同,缺氧段对电子受体的需求不尽相同。刘建广等采用厌氧/缺氧/好氧交替运行模式富集培养DPAOs,发现NO3−-N浓度大于30 mg·L−1时,吸磷速率几乎不受NO3−-N浓度的影响。杨文婷等采用一次性投加硝酸盐,当浓度小于25 mg·L−1时,硝酸盐与磷的去除呈线性关系,每去除1 mg·L−1的NO3−-N同时吸收1.21 mg·L−1的PO43−-P,而ZHOU等得出去除1 mg·L−1的NO3−-N可吸收1.12 mg·L−1的PO43−-P的结论。作为一种新型的反硝化除磷工艺,电子受体对A2/O-MBBR系统中污泥脱氮除磷特性的影响尚不明确。
连续流系统是一个动态变化过程,水质波动较大,多种生化反应交互影响,许多实验现象和微观特性不能直观体现。考虑到连续流系统影响因素的复杂性以及不可控性,本研究以A2/O-MBBR系统长期处理低C/N生活污水的反硝化除磷污泥为研究对象,采用批次实验,考察单因素——不同电子受体浓度对反硝化除磷和动力学特性的影响,从而为A2/O-MBBR系统的工程实践和推广应用提供理论依据。
1 实验部分
1.1 实验装置
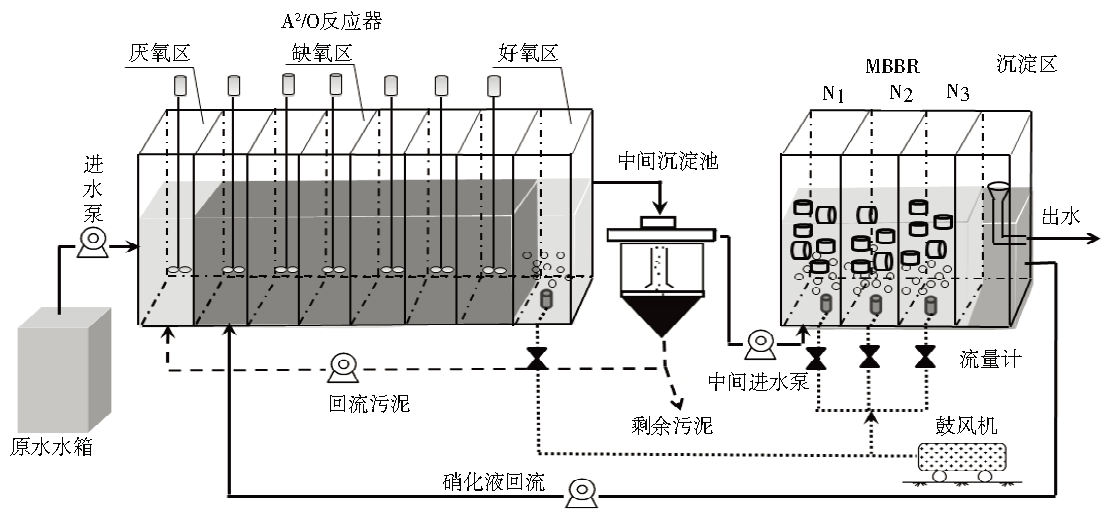
如图1所示,A2/O-MBBR系统由A2/O反应器、中间沉淀池、MBBR、沉淀区顺序连接组成。原水经进水泵进入A2/O反应器,在厌氧区、缺氧区、好氧区的推流作用下完成同步脱氮除磷,出水进入中间沉淀池实现泥水分离。上清液进入MBBR系统,沉淀污泥回流到A2/O反应器的厌氧区(污泥回流比100%)。含有氨氮的上清液在MBBR沿程推流完成氨氮的氧化,硝化液经沉淀区回流到A2/O反应器的缺氧区(硝化液回流比300%),为反硝化除磷过程提供电子受体。
A2/O反应器有效容积28 L,均分为8个格室,水力停留时间8 h,厌氧、缺氧、好氧区容积比为1:6:1;厌氧区和缺氧区内设有搅拌装置,好氧区进行短暂曝气,污泥龄(SRT)控制在10 d左右。中间沉淀池为竖流式,采用中间进水周边出水的运行方式,有效容积10 L,剩余污泥定期排放。MBBR 3格串联,有效容积10.5 L,内设聚丙烯悬浮填料(尺寸D × H为5 mm × 3 mm,填充率50%),溶解氧3.0~4.0 mg·L−1,总曝气量 0.15 m3·h−1左右,主要完成氨氮的氧化,最后出水直接排放。
图1 A2/O-MBBR装置流程图
1.2 污泥特性
A2/O-MBBR系统的接种污泥取自扬州市汤汪污水处理厂CASS反应池的生化污泥,实验用水取自扬州大学生活区的化粪池,进水C/N为2.25~3.40,属于典型的低C/N污水。系统连续运行200 d左右,脱氮除磷性能基本稳定(氮磷去除率分别为80%和96%),进出水的水质特性见表1。采用WACHTMEISTER等推荐的方法得出DPAOs占聚磷菌(PAOs)的比例约为65%,菌群生物活性较好,本研究在此条件下开展了批次实验。
表1 A2/O-MBBR系统进出水水质特性
1.3 批次实验安排
实验污泥取自连续流系统长期稳定运行条件下的活性污泥,用蒸馏水清洗3遍,防止残留基质对反应过程造成不利影响。批次实验分为2个阶段:阶段І,采用人工配水,将清洗后的污泥定容至有效容积5 L的密闭反应瓶中,混合液挥发性悬浮固体浓度(VSS)为3 000 mg·L−1左右,投加乙酸钠后开始厌氧搅拌,在消耗外碳源储存聚-β-羟基链烷酸脂(PHAs)的同时完成释磷过程;阶段Ⅱ,厌氧反应结束后将混合液等分为5份,分别置于有效容积1 L的反应瓶中,投加NO3−-N作为电子受体,以阶段І中的PHAs为电子供体,同步脱氮除磷。
在阶段Ⅱ中,通过改变初始电子受体浓度(NO3−-N:10,20,30,40,50 mg·L−1),探究不同条件下内碳源转化利用情况及其对缺氧反硝化除磷的影响,并通过动力学特性的对比分析阐释脱氮除磷机理。实验在室温(20 ℃)下进行,反应过程中为防止形成聚磷酸盐沉淀,通过投加1 mol·L−1的HCl或NaOH溶液调节pH在7.5左右。
1.4 常规项目监测方法
COD采用快速消解仪(SUNTEXTR-1100)测定;PO43−-P,NO3−-N,NO2−-N等指标以及污泥浓度MLSS、VSS根据标准方法测定;PHAs采用气相色谱(Agilent 6 890N)及DB-1型色谱柱检测;糖原(GLY)采用蒽酮法测定。
1.5 动力学参数计算
在厌氧阶段,DPAOs通过吸收外碳源以PHAs的形式储存在细胞体内,GLY的分解和多聚磷酸盐的水解为此过程提供能量,动力学参数计算如下:
释磷量: QPRA = PAn-t2 − PAn-t1(1)
比释磷速率: RPRR = (PAn-t2 − PAn-t1)/(CVSS-An·ΔTAn) (2)
比耗碳速率: RCUR = (CAn-t1 − CAn-t2)/( CVSS-An·ΔTAn) (3)
在缺氧阶段,DPAOs分解PHAs,以NO3−-N为电子受体同步脱氮除磷,动力学参数计算如下:
反硝化脱氮量: QDNA = NA-t1 − NA-t2(4)
吸磷量: QPUA = PA-t1 − PA-t2(5)
比反硝化速率: RDNR = (NA-t1 − NA-t2)/( CVSS-A·ΔTA) (6)
比吸磷速率: RPUR = (PA-t1 − PA-t2)/( CVSS-A·ΔTA) (7)
式中:CAn-t1、CAn-t2为厌氧阶段t1、t2时刻的COD浓度,mg·L−1;PAn-t1、PAn-t2为厌氧阶段t1、t2时刻的PO43−-P浓度,mg·L−1;PA-t1、PA-t2、NA-t1、NA-t2为缺氧阶段t1、t2时刻的PO43−-P和NO3−-N浓度,mg·L−1;CVSS-An、CVSS-A为厌氧和缺氧阶段的平均污泥浓度,mg·L−1;ΔTAn或ΔTA为t1、t2反应时间间隔,h。
2 结果与讨论
2.1 实验条件的选择和确定
2.1.1 碳源投加量及厌氧反应时间
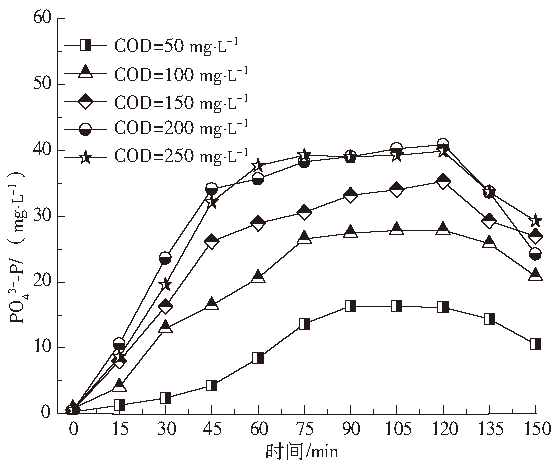
如图2所示,当乙酸钠(以COD计)浓度在50~250 mg·L−1变化时,释磷量随着反应时间的进行不断增加,但在90~20 min之间出现释磷平台,最高PO43−-P浓度分别为16.35、27.88、35.29、40.88和39.24 mg·L−1,随后PO43−-P含量均呈现下降趋势。由于DPAOs吸收外碳源合成PHAs的能力存在极限值,一旦PHAs合成量达到最大值,便不再利用外碳源,导致高COD浓度时出现无效释磷;而厌氧反应时间过长容易导致微生物暴露于饥饿状态,出现吸磷现象。本实验条件下,最佳乙酸钠投加量和厌氧反应时间分别为200 mg·L−1、90 min。
图2 不同COD浓度下释磷情况
2.1.2 缺氧反应时间
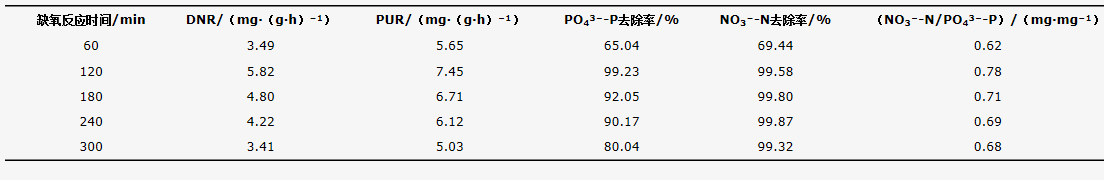
由于反硝化除磷主要在缺氧段完成,维持适当的缺氧反应时间对保证良好的脱氮除磷效果至关重要。表2对比了缺氧反应时间60~300 min的反硝化除磷特性(初始NO3−-N、PO43−-P浓度分别为(35 ± 2) mg·L−1、(40 ± 3) mg·L−1),当缺氧反应时间120 min时,同步脱氮除磷性能最佳(均超过99%),PUR为7.45 mg·(g·h)−1,DNR为5.82 mg·(g·h)−1,平均每吸收1 mg PO43−-P可去除0.78 mg NO3−-N。缺氧反应时间过短,反硝化吸磷不充分;缺氧反应时间过长,微生物因电子供体、电子受体消耗殆尽而处于饥饿状态,生物活性下降,甚至发生2次释磷现象。
表2 不同缺氧反应时间下的反硝化除磷特性
综上,确定本研究的实验条件:阶段І,投加200 mg·L−1乙酸钠,厌氧反应时间90 min;阶段Ⅱ,投加电子受体NO3−-N,缺氧反应时间120 min。在此基础上,考察不同NO3−-N浓度(10~50 mg·L−1)条件下的反硝化除磷特性。具体联系污水宝或参见http://www.dowater.com更多相关技术文档。
2.2 厌氧释磷及碳源的转化利用
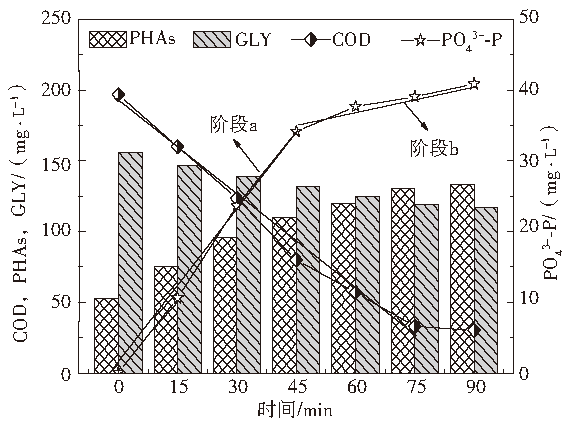
如图3所示,厌氧初始时刻COD浓度为196.72 mg·L−1,随着反应的进行,COD浓度快速降低,到75~90 min时,COD浓度从32.10 mg·L−1降为30.61 mg·L−1,可利用外碳源基本消耗殆尽。与此同时,PHAs与GLY含量此消彼长,PHAs含量从53.11 mg·g−1增加至133.40 mg·g−1,90 min时几乎全部外碳源都以PHAs的形式储存于细胞体内,同时伴随着少量GLY分解(浓度从156.21 mg·g−1降为117.36 mg·g−1)。整个过程COD利用率为84.57%,比耗碳速率为36.91 mg·(g·h)−1。
图3 厌氧阶段碳源转化与释磷情况
此外,碳源转化利用过程中,释磷速率出现明显的分界(阶段a和阶段b),PO43−-P浓度从初始时刻的0.07 mg·L−1快速上升,45 min时增大到34.13 mg·L−1;在随后的45~90 min内,PO43−-P浓度增加缓慢,增幅仅为6.75 mg·L−1。2个阶段PRR分别为15.14 mg·(g·h)−1和3.0 mg·(g·h)−1,与图3中内碳源PHAs(ΔPHAs=57.26、23.04 mg·g−1)和GLY(ΔGLY=24.61、14.24 mg·g−1)的变化利用规律相吻合。阶段a中PHAs合成量是阶段b的2.49倍,表明厌氧45 min后虽然COD浓度一直在降,但是内碳源的转化效率已经不高。内碳源转化和释磷情况均表明,厌氧90 min已实现最优的处理效果。WANG等在A2N-SBR中同样发现厌氧反应时间90 min时,系统合成的PHAs含量最高,氮磷去除率分别达到91%,94%;并且当厌氧反应时间延长,PHAs含量的降低导致缺氧段PHAs分解效率下降,出现游离亚硝酸积累,脱氮除磷效果变差。
2.3 缺氧反硝化除磷特性
2.3.1 不同NO3−-N浓度下的脱氮除磷特性
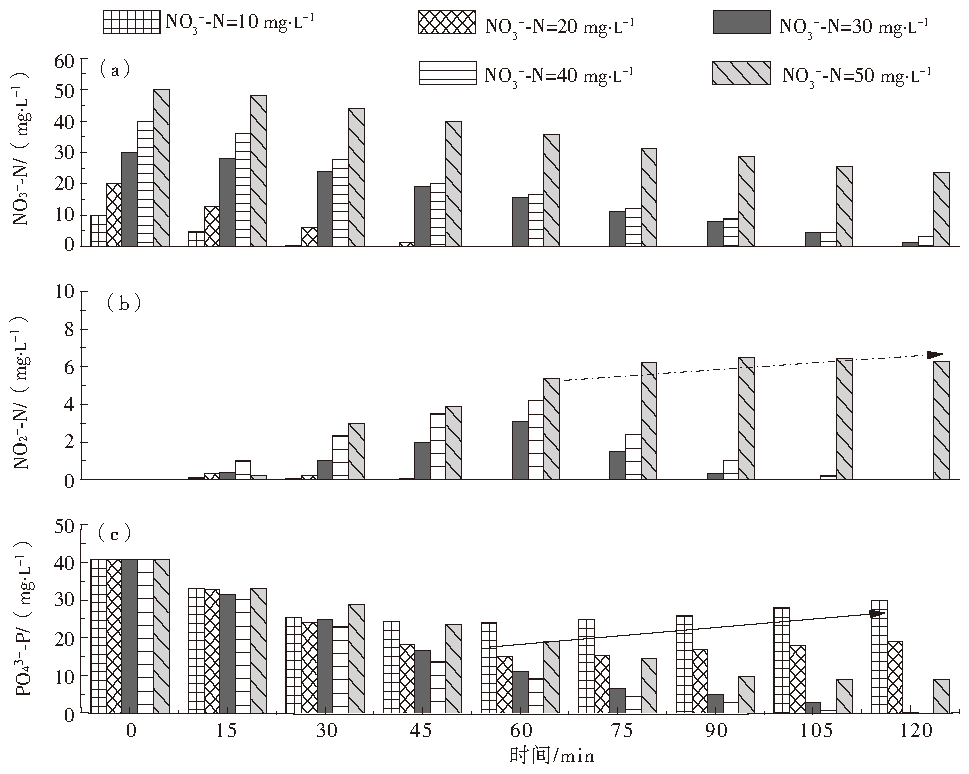
在图4中,当NO3−-N浓度为10 mg·L−1和20 mg·L−1时,NO3−-N在45~60 min内反应完全,且整个过程NO2−-N积累很微弱(0.05~0.2 mg·L−1),基本可以忽略不计;但由于电子受体不足导致吸磷受限,到60 min时,PO43−-P浓度分别残留23.98 mg·L−1和15.14 mg·L−1,后续反应过程都出现不同程度的2次释磷现象(如图4(c)箭头所示)。
NO3−-N浓度增加到30 mg·L−1,反应时间120 min时NO3−-N和PO43−-P浓度为1.09 mg·L、0.25 mg·L−1,去除率分别为96.37%和99.39%,实现了同步高效脱氮除磷。当NO3−-N增加到40 mg·L−1,电子受体有部分剩余,反应结束时NO3−-N仍残留3.09 mg·L−1,但PO43−-P在反应时间105 min时已完全去除,氮磷去除率分别为92.28%和100%。此外,上述2种工况在前60 min均出现不同程度的NO2−-N积累,最高可达到3.12 mg·L−1和4.26 mg·L−1,但在后续反应NO2−-N被逐步反硝化,且除磷效果基本不受影响。
而当NO3−-N浓度增加到50 mg·L−1时,整个反应过程伴随着明显的NO2−-N积累,到90 min时,NO2−-N浓度高达6.5 mg·L−1且后续略有上升趋势(如图4(b)箭头所示)。ZHOU等和JABARI等均发现,NO2−-N的存在会抑制DPAOs的生物活性且限制同步脱氮除磷效率,到反应结束时NO3−-N和PO43−-P浓度分别为23.38 mg·L−1和9.05 mg·L−1,去除率仅为53.24%和77.86%。
图4 NO3−-N浓度对脱氮除磷效果的影响
单从脱氮除磷效率看,在本研究条件下(取自A2/O-MBBR系统的反硝化除磷污泥,DPAOs占PAOs比例约为65%),以NO3−-N为电子受体进行反硝化除磷时,当NO3−-N投加量为30 mg·L−1时较为合适,与傅金祥等[17]的研究结论相同,即硝酸盐型反硝化除磷过程最佳电子受体投加量为30 mg·L−1时,DPAOs能最大程度地利用NO3−-N进行同步脱氮除磷。
2.3.2 不同NO3−-N浓度下的内碳源转化利用特性
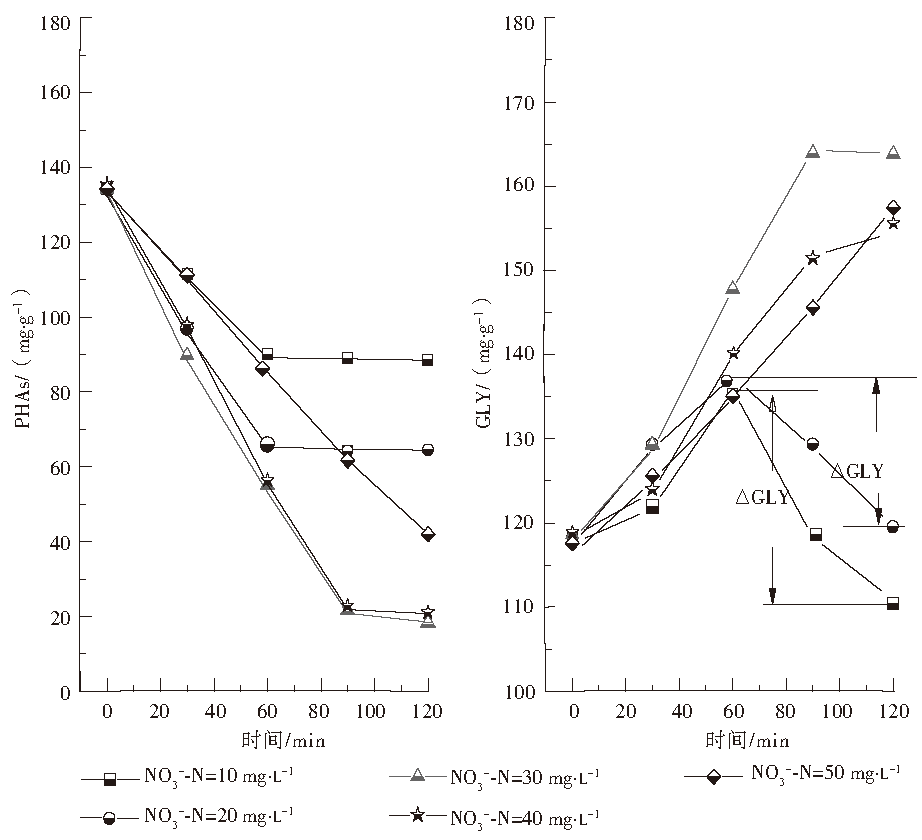
为了进一步考察不同NO3−-N浓度条件下的反硝化除磷特性,图5对比了内碳源PHAs和GLY的转化利用情况(其中缺氧初始时刻PHAs、GLY的含量分别为132.4~134.5 mg·g−1和116.2~118.36 mg·g−1 )。当NO3−-N浓度为10 mg·L−1和20 mg·L−1时,前阶段NO3−-N的快速反应伴随着PHAs的消耗和GLY的合成,反应60 min时GLY含量分别为134.80 mg·g−1和138.41 mg·g−1,PHAs含量分别为89.15 mg·g−1和65.30 mg·g−1,且PHAs在后续反应中基本保持不变;但60 min后,虽然NO3−-N消耗完全,GLY却存在降解的趋势,2种工况ΔGLY分别为25.06 mg·g−1和17.8 mg·g−1 (见图5)。BASSIN等认为当电子供体或电子受体消耗殆尽时,微生物会由于处于饥饿状态而出现GLY降解的现象,长期运行对DPAOs的生长富集是不利的。
图5 NO3−-N浓度对PHAs和GLY转化利用特性的影响
当NO3−-N浓度为30 mg·L−1和40 mg·L−1时,整个反应过程PHAs和GLY此消彼长,PHAs的减少量分别为114.92 mg·g−1和110.77 mg·g−1,GLY的增加量分别为55.98 mg·g−1和69.16 mg·g−1。由于微生物体内需保持一定量的PHAs来维持自身的生命活动,反应结束120 min时,PHAs的含量为18.48~20.73 mg·g−1,PHAs利用率为84.6%~86.2%。研究表明改良UCT分段进水工艺中出水PHAs含量为0.8~1.1 mmol·L−1(相当于13~19 mg·g−1)时,系统展现出较好的反硝化除磷性能。
当NO3−-N浓度增加到50 mg·L−1时,NO3−-N负荷的增加以及NO2−-N积累(见图4(b))导致DPAOs生物活性下降,同样限制了内碳源转化利用效率,反应结束时出水中PHAs仍残留42.10 mg·g−1,PHAs利用率仅为68.4%,造成内碳源的浪费,该结果与2.3.1中脱氮除磷效率的下降相吻合。综合脱氮除磷效果以及内碳源转化效率,在本研究的特定条件下,当NO3−-N浓度为30~40 mg·L−1时较为适宜。
2.4 反硝化除磷的动力学分析
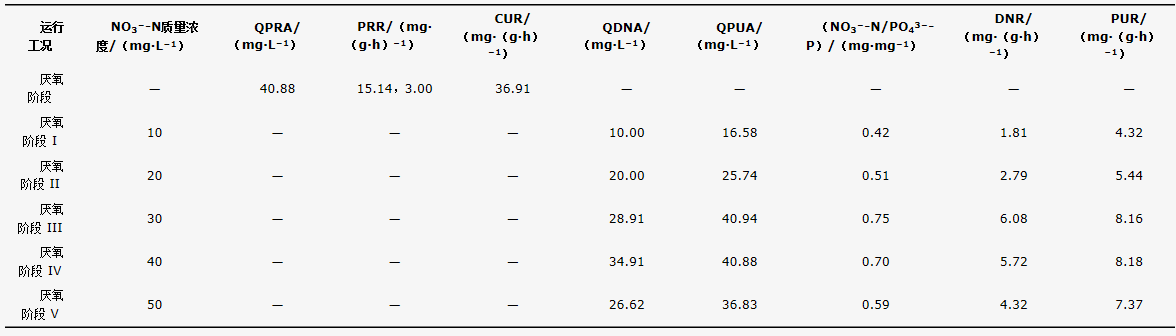
结合式(1)~式(7),表3对比了厌氧阶段以及缺氧阶段不同NO3−-N浓度下的反硝化除磷动力学参数。厌氧释磷过程较高的CUR促进了磷酸盐的快速分解,PRR最高达15.14 mg·(g·h)−1,不同NO3−-N浓度下缺氧吸磷过程PUR为4.32~8.18 mg·(g·h)−1,电子受体不足(NO3−-N浓度为10~20 mg·L−1)或电子受体过剩(NO3−-N浓度为50 mg·L−1)均不利于吸磷反应的进行。PENG等[3]考察了A2/O分段进水和UCT工艺的反硝化除磷特性,2种工艺中PRR和PUR分别为4.44 mg·(g·h)−1、1.33 mg·(g·h)−1和7.91 mg·(g·h)−1、3.19 mg·(g·h)−1。对比结果表明,A2/O-MBBR系统的污泥体现了优越的反硝化除磷性能,意味着双污泥系统中DPAOs具有较高的生物活性。
表3 不同运行工况下的反硝化除磷动力学参数
缺氧阶段NO3−-N浓度与反硝化除磷特性密切相关,DNR一定程度上反映了DPAOs的反硝化潜力。当NO3−-N浓度为30 mg·L−1和40 mg·L−1时,DNR达到了最高值5.72~6.08 mg·(g·h)−1,而NO3−-N浓度为10 mg·L−1时,DNR仅为1.81 mg·(g·h)−1,但该结果依然高于某PAOs富集的生物膜系统(DNR=1.45 mg·(g·h)−1)[21]。除此之外,NO3−-N/PO43−-P比值与NO3−-N负荷也呈现相关性,间接反映了DPAOs的反硝化除磷潜力。反硝化除磷过程平均吸收1 mg PO43−-P 可去除0.42~0.75 mg NO3−-N,高于完全混合式SNDPR系统(0.33 mg NO3−-N)以及悬浮污泥和生物膜共存的IFAS系统(0.41~0.72 mg NO3−-N)。双污泥系统中DPAOs和硝化菌的分离、富集,是提高反硝化除磷性能的主要原因,上述分析进一步验证了A2/O-MBBR系统在处理低C/N比污水方面的优越性。
3 结论
1)乙酸钠投加量200 mg·L−1,厌氧反应时间90 min时释磷完全,PO43−-P浓度最高可达40.88 mg·L−1,PHAs合成量为133.40 mg·g−1,比耗碳速率为36.91 mg·(g·h)−1;缺氧反应时间120 min时,可获得最佳的同步脱氮除磷效果。
2)厌氧释磷速率在45 min时出现明显的分界,2个阶段的释磷速率分别为15.14 mg·(g·h)−1和3.0 mg·(g·h)−1,前者PHAs合成量是后者的2.49倍。
3)在本研究条件下,缺氧段NO3−-N浓度为30 mg·L−1时,可实现同步高效脱氮除磷,氮磷去除率分别为96.37%和99.39%。NO3−-N浓度增加到40 mg·L−1时,PHAs利用率从84.6%上升为86.2%且除磷效果不受影响,得出NO3−-N的最佳投加量为30~40 mg·L−1。
4)反硝化除磷过程最高PUR为8.16~8.18 mg·(g·h)−1,DNR高达5.72~6.08 mg·(g·h)−1,吸收1 mg PO43−-P 可去除0.42~0.75 mg NO3−-N,处理性能优于传统反硝化除磷工艺,揭示了A2/O-MBBR系统中DPAOs较高的生物活性。(来源:环境工程学报 作者:张淼)