染料废水具有污染物浓度高、色度深、难生物降解等特点,易引发许多环境污染问题。在探寻高效、经济地处理染料废水的诸多方法中,Fenton试剂氧化法因其反应速率快、操作简单等优点备受重视。但是传统的Fenton试剂氧化体系需要在较低的pH范围(小于4)内反应,且铁离子的分离和重复利用也受到一定限制。为了在更宽的pH范围内进行反应并使催化剂得到充分利用,更多的研究趋向于非均相Fenton试剂氧化反应催化剂的研制。由于Fe在自然界含量丰富,对环境无毒,Fe- H2O2 体系及其耦合技术被广泛研究,如Lucking等以H2O2为氧化剂,以Fe粉、石墨、活性炭为催化剂降解水中的4-氯酚,他们认为Fe粉可以代替Fe盐作为Fenton试剂氧化反应的催化剂。此外,微波技术也广泛应用于有机物的降解中,微波不仅能改变体系的热力学函数,降低反应的活化能和分子的化学键强度,还可以促进一些难以进行的反应的发生,因此微波技术在化学合成、环境工程领域得到了广泛的应用。
本工作以罗丹明B模拟废水为处理对象,考察微波辅助Fe-H2O2协同作用对高浓度罗丹明B废水的脱色效果,并探讨了不同影响因素对罗丹明B去除效果的影响。
1 实验部分
1.1 试剂和仪器
罗丹明B:分析纯;双氧水:质量分数30%,分析纯;Fe粉:过100目筛,分析纯。
pH S-3S型pH计:上海理达仪器厂;UV-2450型紫外-可见分光光度计:日本岛津公司;微波反应器:格兰仕微波炉自行改装。
1.2 实验方法
取200 mL一定质量浓度的废水,用浓度为0.1mol/L的HNO3溶液或浓度为0.1 mol/L 的NaOH溶液调节废水pH,加入Fe粉和质量分数30%的H2O2。在300 W微波辐射下反应一段时间,取样分析。测定时将废水稀释10倍,于波长552 nm处测其吸光度。
2 结果与讨论
2.1 废水pH对罗丹明B去除率的影响
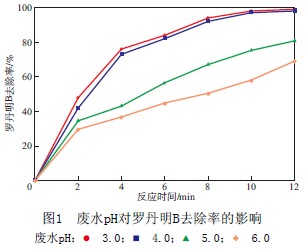
当初始罗丹明B质量浓度为100 mg/L、Fe粉加入量为50 mg/L、H2O2加入量为10.0 mL/L时,废水pH对罗丹明B去除率的影响见图1。由图1可见:当废水pH为3.0和4.0时,罗丹明B去除率随反应时间延长而迅速增大,废水脱色完全;随着废水pH升高,罗丹明B去除率减小,脱色速率变慢。这是由于废水pH影响了Fe在水溶液中的化学反应。当废水pH较低时,Fe被氧化成Fe2+,Fe2+进而与H2O2作用生成羟基自由基,从而氧化去除罗丹明B;而在较高pH条件下,铁离子的水解作用成为主要反应,Fe的氢氧化物沉淀附着于Fe粉的表面,阻碍了Fe2+的溶出以及Fe3+的循环利用。同时,H2O2在强碱性条件下较易分解,不利于其利用。
一般认为传统Fenton试剂氧化法的最佳pH为3.0,且都是在酸性条件下才能进行。而微波辅助Fe-H2O2体系能够在废水pH为4.0时仍能达到较快较好的处理效果,反应12 min时罗丹明B的去除率为98.7%,故在该体系下Fenton试剂氧化反应的pH范围比传统的Fenton试剂氧化反应宽。
2.2 H2O2加入量对罗丹明B去除率的影响
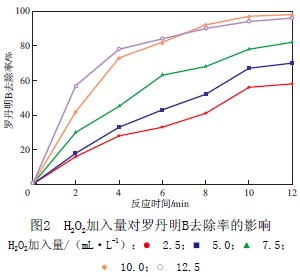
当初始罗丹明B质量浓度为100 mg/L、废水pH为4.0、Fe粉加入量为50 mg/L时,H2O2加入量对罗丹明B去除率的影响见图2。由图2可见:随着H2O2加入量的增加,罗丹明B去除率增大;当H2O2加入量小于10.0 mL/L时,罗丹明B不能被完全去除,这主要是由于当H2O2较少时废水中没有足够的Fe2+产生,但随着H2O2加入量增加到12.5 mL/L时,罗丹明B去除率较H2O2加入量为10.0 mL/L时未有明显改变。当投加过量的H2O2时,H2O2 同时会充当自身的消除剂,从而减少了废水中羟基自由基的量。因此,在本实验中,H2O2的最佳加入量为10.0 mL/L。
2.3 Fe粉加入量对罗丹明B去除率的影响
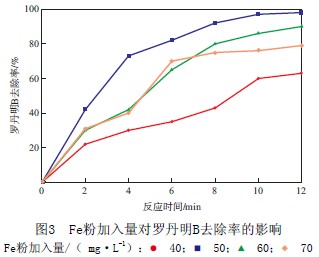
当初始罗丹明B质量浓度为100 mg/L、废水pH为4.0、H2O2的加入量为10.0 mL/L时,Fe粉加入量对罗丹明B去除率的影响见图3。由图3可见:当Fe粉加入量为40 mg/L时,罗丹明B的去除率较低;当Fe粉加入量为50 mg/L时,反应时间相同时,罗丹明B去除率最大,说明去除速率较快;当Fe粉加入量继续增大时,罗丹明B去除率减小,去除效果下降。这种现象主要是因为Fe粉的加入量不同,影响Fe2+的溶出,而过量的Fe2+同样会成为羟基自由基的消除剂。在本实验中,Fe粉最佳加入量为50 mg/L。
2.4 初始罗丹明B质量浓度对罗丹明B去除率的影响
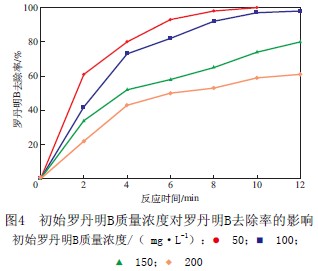
当废水pH为4.0、H2O2的加入量为10.0 mL/L、Fe粉加入量为50 mg/L时,初始罗丹明B质量浓度对罗丹明B去除率的影响见图4。由图4可见:随着初始罗丹明B质量浓度的增加,其去除率减小;当初始罗丹明B质量浓度为50 mg/L、反应10 min时,罗丹明B的去除率已达到100%,当初始罗丹明B质量浓度分别为100,150,200 mg/L时,反应12 min罗丹明B的去除率分别为98.7%,74.5%,59.8%。这主要是由于初始罗丹明B质量浓度高,废水中羟基自由基及其他氧化剂含量相对较少,同时,降解过程中的中间产物的量也会较多,导致罗丹明B去除速率下降。
2.5 对比实验
在上述最佳实验条件下,不同反应体系对罗丹明B去除率的影响见图5。
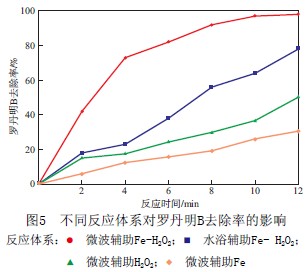
由图5可见,在水浴辅助Fe-H2O2、微波辅助H2O2和微波辅助Fe体系中各反应12 min后,罗丹明B去除率分别达到78.1%,50.2%,30.8%,远远低于微波辅助Fe-H2O2体系对罗丹明Bz的去除率,可见微波对Fe-H2O2处理罗丹明B的去除具有较强的辅助作用。
在微波辅助Fe体系中,微波作用于Fe粉能引起其表面迅速升温,1 min能达到370~540 ℃。高温和酸性环境改变了Fe粉表面性质,并吸附部分罗丹明B,这两方面作用使溶液中罗丹明B部分降解。在微波辅助 H2O2体系下,罗丹明B的去除率为50.2%,这是因为H2O2在微波辐射下能够产生包括羟基自由基在内的一些自由基,可使罗丹明B降解。
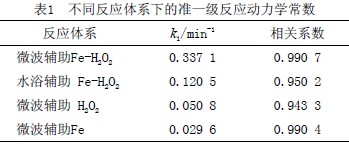
对不同反应体系中罗丹明B的去除反应进行了动力学拟合,结果为准一级动力学。不同反应体系下的准一级反应动力学常数见表1。由表1可见,微波辅助Fe-H2O2体系降解罗丹明B的k1远远大于其他反应体系。在微波的作用下,降低了微波辅助Fe-H2O2体系的反应活化能,并且使Fe和H2O2反应加快,促进羟基自由基的生成,加速罗丹明B的去除。
2.6 Fe粉的重复使用
在微波辅助Fe-H2O2体系最佳实验条件下进行Fe粉重复利用实验。反应时间为12 min,每一次实验完成后,倾出反应液,再加入废水和H2O2。经5次实验,罗丹明B去除率接近100%,反应器底部仍有Fe粉残留。
2.7 微波辅助Fe-H2O2体系中罗丹明B废水的紫外光谱
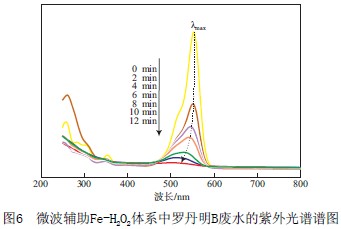
罗丹明B具有一个氧杂蒽环结构,在环的两边是N-乙烷基,这种特殊的结构使它在水溶液中相对稳定。微波辅助Fe-H2O2体系不同反应时间时罗丹明B废水的紫外光谱谱图见图6。由图6可见:罗丹明B在553 nm处具有最大吸收峰;随着反应时间的延长,废水的最大吸收峰值明显减小,且最大吸收波长发生了一定的蓝移,最大吸收峰逐步从553 nm偏移到520 nm左右,废水的颜色也由原来的红色逐渐变为无色。Hu等认为这种蓝移现象是由于罗丹明B经一系列脱乙基反应后产生的中间产物形成的。因此,在微波辅助Fe-H2O2体系中,罗丹明B结构的脱乙基过程是主要的降解过程。
3 结论
a)微波辅助Fe-H2O2体系联合处理罗丹明B废水,可提高罗丹明B去除率和去除速率,同时在该体系下Fenton试剂氧化反应的pH范围较传统的Fenton试剂氧化反应要宽。具体参见http://www.dowater.com更多相关技术文档。
b)Fe粉、H2O2的加入量存在一个临界值,当加入量高于临界值时,罗丹明B去除率不增反降。最佳实验条件为废水pH为4.0,Fe粉加入量为50 mg/L,H2O2加入量为10.0 mL/L。对于初始罗丹明B质量浓度为100 mg/L的废水,在此条件下反应12 min,罗丹明B的去除率达到98.7%。
c)Fe粉可多次使用。经5次使用时,反应12min后罗丹明B去除率接近100%。
